Rapport 2024 sur le paludisme dans le monde - Principaux messages (Focus Afrique)
Les ripostes au paludisme mises en œuvre dans le monde entier préviennent la maladie et sauvent des vies
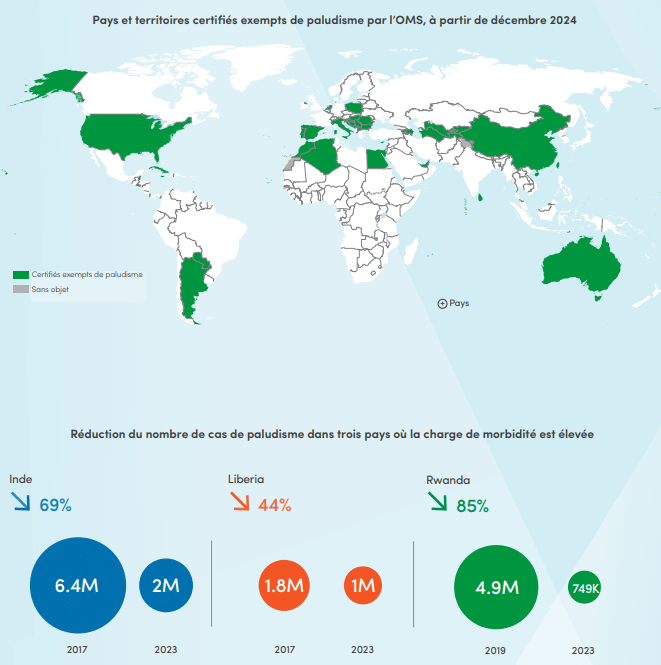 Depuis 2000, les efforts déployés pour lutter contre le paludisme ont permis d'éviter 2,2 milliards de cas et 12,7 millions de décès dans le monde. En plus de diverses interventions ciblées, d'autres facteurs tels que les améliorations des conditions socioéconomiques, ainsi que dans les domaines de la nutrition, des infrastructures, de l'habitat et de l'urbanisation ont vraisemblablement aidé à réduire la transmission et le poids du paludisme.
Depuis 2000, les efforts déployés pour lutter contre le paludisme ont permis d'éviter 2,2 milliards de cas et 12,7 millions de décès dans le monde. En plus de diverses interventions ciblées, d'autres facteurs tels que les améliorations des conditions socioéconomiques, ainsi que dans les domaines de la nutrition, des infrastructures, de l'habitat et de l'urbanisation ont vraisemblablement aidé à réduire la transmission et le poids du paludisme.
Des progrès ont été enregistrés dans de nombreux pays, l'OMS a certifié 44 pays et 1 territoire exempts de paludisme, y compris très récemment l'Égypte et certains pays à charge palustre élevée réalisent également des progrès remarquables :
Dans la région Afrique de l'OMS, le Rwanda a réduit de 85 % son nombre de cas de paludisme entre 2019 et 2023, passant de 4,9 millions de cas estimés à 749 000, alors que le Libéria a enregistré une diminution de 44 % de son nombre de cas depuis 2017, soit une baisse de 1,8 million à 1 million. Dans la région Asie du Sud Est, l'Inde a réduit son nombre de cas de 69 %, avec 6,4 millions de cas en 2017 contre 2 millions en 2023. Voir l'infographie

Masquer l'infographie
Toutefois, le paludisme reste un défi majeur de santé mondiale, surtout dans la région Afrique déjà durement touchée
En 2023, le nombre des nouveaux cas de paludisme estimés a atteint 263 millions dans 83 pays à travers le monde, contre 252 millions en 2022 et 226 millions en 2015. Entre 2022 et 2023, l'Éthiopie (+4,5 millions), Madagascar (+2,7 millions), le Pakistan (+1,6 million), le Nigéria (+1,4 million) et la République démocratique du Congo (+600 000) sont les pays qui ont le plus largement contribué à cette hausse. L'incidence du paludisme, qui est liée à la croissance démographique, a augmenté durant la période 2015–2023, passant de 58 à 60,4 cas pour 1 000 habitants exposés au risque de paludisme.
Le nombre total de décès dus au paludisme dans le monde s'est élevé à 597 000 en 2023 contre 578 000 en 2015. En 2020, les perturbations causées par la pandémie de COVID-19 ont entraîné une forte hausse des décès associés au paludisme, avec 55 000 morts supplémentaires. Le nombre total de décès a réduit progressivement durant les années postCOVID, tout comme le taux de mortalité.
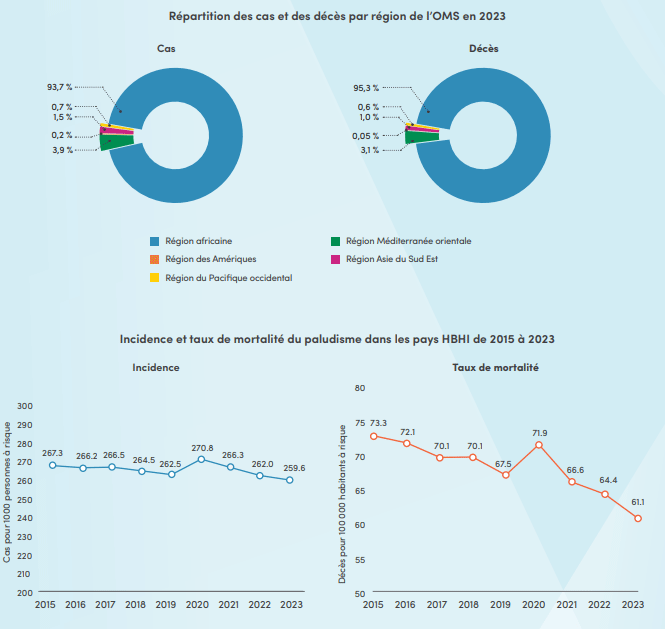
La région Afrique paye toujours le plus lourd tribut, cumulant à elle seule 94 % du nombre total des cas et 95 % des décès associés au paludisme au niveau mondial selon les estimations de 2023. Un peu plus de la moitié de ces décès ont été enregistrés dans quatre pays : Niger (5,9%), Nigéria (30,9%), République démocratique du Congo (11,3%) et République-Unie de Tanzanie (4,3%).
Bien que la riposte au paludisme en Afrique ait remporté quelques succès, il est temps de progresser plus rapidement
 Près des deux tiers des nombres de cas de paludisme et de décès associés au niveau mondial sont concentrés dans 11 pays d'Afrique : Burkina Faso, Cameroun, Ghana, Mali, Mozambique, Niger, Nigéria, Ouganda, Soudan, République démocratique du Congo et République-Unie de Tanzanie. Ces 11 pays ont adopté l'approche « D'une charge élevée à un fort impact » (HBHI), une riposte ciblée ayant pour objet d'atteindre les populations exposées au risque de paludisme le plus élevé grâce à des ensembles d'interventions adaptés sur mesure, tenant compte des données locales et des conditions spécifiques.
Près des deux tiers des nombres de cas de paludisme et de décès associés au niveau mondial sont concentrés dans 11 pays d'Afrique : Burkina Faso, Cameroun, Ghana, Mali, Mozambique, Niger, Nigéria, Ouganda, Soudan, République démocratique du Congo et République-Unie de Tanzanie. Ces 11 pays ont adopté l'approche « D'une charge élevée à un fort impact » (HBHI), une riposte ciblée ayant pour objet d'atteindre les populations exposées au risque de paludisme le plus élevé grâce à des ensembles d'interventions adaptés sur mesure, tenant compte des données locales et des conditions spécifiques.
L'incidence de la maladie (cas pour 1 000 habitants exposés au risque de paludisme) et les taux de mortalité (décès pour 100 000 habitants exposés au risque de paludisme) dans les 11 pays HBHI ont respectivement reculé de 3 % et 13 % entre 2017 et 2023.
De 2015 à 2023, la région Afrique dans son ensemble a réussi à réduire de 5 % l'incidence de la maladie et de 16 % les taux de mortalité. Toutefois, les chiffres de 2023 pour ces deux indicateurs équivalaient encore à plus du double des cibles fixées par la Stratégie mondiale. Voir l'infographie

Masquer l'infographie
2. Principales menaces pesant sur les progrès Voir le chapitre 2
 Au lendemain de la pandémie de COVID-19, les pays d'endémie palustre font face à des défis persistants. La fragilité des systèmes de santé, l'insuffisance de la surveillance et le manque chronique de fonds demeurent des obstacles majeurs.
Au lendemain de la pandémie de COVID-19, les pays d'endémie palustre font face à des défis persistants. La fragilité des systèmes de santé, l'insuffisance de la surveillance et le manque chronique de fonds demeurent des obstacles majeurs.
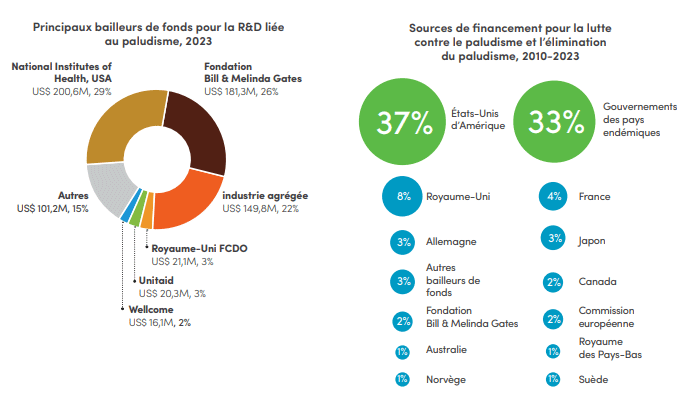
En 2023, les fonds disponibles sont restés nettement inférieurs à l'objectif de US$ 8,3 milliards
Au niveau mondial, les investissements dans la lutte contre le paludisme ont totalisé, selon les estimations, US$ 4 milliards en 2023, un chiffre bien en-deçà de l'objectif de US$ 8,3 milliards fixé dans la Stratégie mondiale de lutte contre le paludisme. Le déficit de financement s'est accentué ces cinq dernières années, passant de US$ 2,6 milliards en 2019 à US$ 4,3 milliards en 2023. Voir l'infographie

Masquer l'infographie
Les urgences humanitaires augmentent les risques de paludisme dans de nombreux pays endémiques
En Éthiopie, le nombre de cas de paludisme estimés a également plus que triplé, passant de 2,6 millions en 2019 à 9,5 millions en 2023. Ces dernières années, les services de santé de base et les mesures de prévention du paludisme ont été perturbés dans les zones de conflit et le pays a dû faire face à d'autres défis, y compris l'émergence du moustique Anopheles stephensi, la résistance aux insecticides et les effets du changement climatique.
Le changement climatique menace les avancées réalisées dans la lutte contre le paludisme
Les températures en hausse et l'évolution des phénomènes météorologiques nuisent à la santé, à la sécurité et aux moyens de subsistance des populations dans le monde entier. Les premières victimes des effets les plus graves du changement climatique sont les communautés vulnérables en Afrique et plusieurs d'entre elles sont déjà plus exposées au risque de contracter le paludisme.
De nombreuses populations exposées au risque de paludisme n'ont toujours pas accès aux services essentiels de prévention, diagnostic et traitement du paludisme
En 2023 par exemple, plus de 40 % des enfants de moins de cinq ans ainsi que des jeunes filles et femmes enceintes en Afrique subsaharienne n'ont pas dormi sous une moustiquaire imprégnée d'insecticide, qui est portant un outil essentiel de prévention du paludisme.
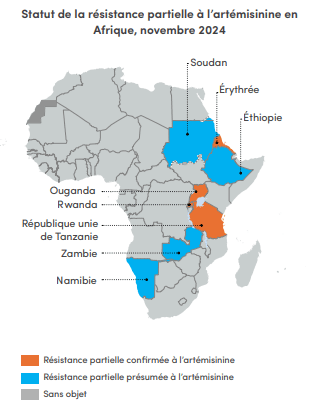 En Afrique, la propagation de la résistance aux médicaments antipaludiques est une vive source d'inquiétude
En Afrique, la propagation de la résistance aux médicaments antipaludiques est une vive source d'inquiétude
À ce jour, quatre pays d'Afrique de l'Est confirment la présence d'une résistance partielle à l'artémisinine (Érythrée, Ouganda, RépubliqueUnie de Tanzanie et Rwanda). En se basant sur les données disponibles, la même résistance est également suspectée dans quatre autres pays (Éthiopie, Namibie, Soudan et Zambie).
En 2022, l'OMS a lancé une stratégie visant à freiner la résistance aux antipaludiques en Afrique. Cette stratégie s'appuie sur les leçons tirées des plans d'action mondiaux du passé et complète les stratégies existantes, en y incluant des efforts plus intenses pour faire face à la résistance antimicrobienne.
Les quatre piliers de la « Stratégie de riposte face à la résistance aux antipaludiques en Afrique » :
- Renforcer la surveillance de la résistance aux antipaludiques et de leur efficacité ;
- Optimiser et mieux réglementer l'usage des produits de diagnostic et des moyens thérapeutiques pour limiter la pression médicamenteuse en prenant des mesures préemptives ;
- Réagir à la résistance en limitant la propagation des parasites résistant aux antipaludiques ;
- Stimuler la recherche et l'innovation afin de mieux exploiter les outils existants et mettre au point de nouveaux outils contre la résistance.
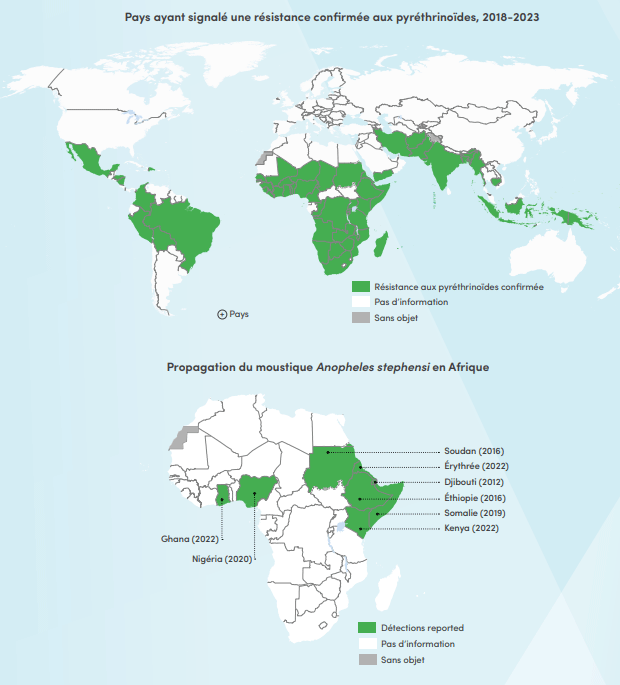 La résistance des moustiques aux pyréthrinoïdes reste très répandue
La résistance des moustiques aux pyréthrinoïdes reste très répandue
La résistance aux pyréthrinoïdes, le produit chimique le plus couramment utilisé sur les moustiquaires imprégnées d'insecticide, a été confirmée dans 55 des 64 pays où elle a été surveillée de 2018 à 2023. Les moustiquaires de nouvelle génération, qui offrent une meilleure protection contre le paludisme que les moustiquaires imprégnées uniquement de pyréthrinoïdes, sont de plus en plus souvent disponibles et constituent un outil important intégré aux efforts de lutte contre le paludisme à l'échelle mondiale. L'OMS a publié des recommandations concernant leur utilisation en 2017 et 2023, respectivement.
Le moustique Anopheles stephensi présente un défi supplémentaire pour la lutte contre le paludisme en Afrique
Originaires d'Asie du Sud et de la péninsule arabique, les espèces de moustiques invasives se sont répandues au cours de la dernière décennie et ont été détectées dans huit pays d'Afrique. An. stephensi peut se développer en milieux urbains, résiste à de fortes températures ainsi qu'à de nombreux insecticides utilisés dans le domaine de la santé publique. En 2022, l'OMS a lancé une initiative [en anglais uniquement] dans le but de sensibiliser ses États membres et partenaires à cette menace croissante et de catalyser les efforts déjà déployés pour stopper la propagation d'An. stephensi en Afrique. Voir l'infographie

Masquer l'infographie
3. Quels sont les progrès accomplis ? Voir le chapitre 3
Le rapport 2024 met en avant les tendances positives enregistrées concernant l'intensification des outils de prévention efficaces, notamment les moustiquaires de nouvelle génération, les vaccins contre le paludisme et la chimioprévention du paludisme saisonnier.
Des progrès significatifs ont également été réalisés dans le domaine des services précoces de diagnostic et de traitement auprès des jeunes enfants. Toutefois, la couverture des moustiquaires imprégnées d'insecticide (MII) et des traitements préventifs du paludisme chez les jeunes filles et femmes enceintes accuse toujours du retard et les zones affichant les chiffres les plus bas nécessitent des mesures complémentaires.
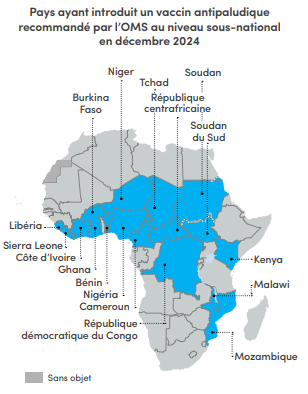 Le déploiement plus important des vaccins promet également d'alléger le fardeau de la maladie en Afrique
Le déploiement plus important des vaccins promet également d'alléger le fardeau de la maladie en Afrique
L'utilisation de deux vaccins antipaludiques, RTS,S/AS01 (RTS,S) et R21/Matrix-M, est désormais recommandée par l'OMS dans les zones d'endémie palustre. De 2019 à 2023, près de 2 millions d'enfants au Ghana, au Kenya et au Malawi ont été vaccinés avec RTS,S. Une évaluation de l'impact a révélé une réduction de 13 % du taux de mortalité toutes causes confondues (à l'exclusion des blessures) et de 22 % des hospitalisations pour paludisme grave chez des enfants admissibles en âge à la vaccination durant cette période.
L'intensification de la vaccination antipaludique en Afrique devrait sauver des dizaines de milliers de jeunes vies chaque année. L'impact maximal sera atteint dès que les vaccins seront administrés parallèlement à une combinaison d'autres interventions de lutte contre le paludisme recommandées par l'OMS et adaptées aux conditions locales.
Le déploiement des moustiquaires de nouvelle génération a grandement progressé ces dernières années
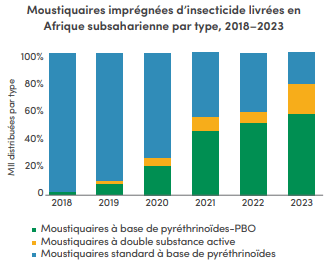 À ce jour, plus de 3 milliards de moustiquaires imprégnées d'insecticide ont été distribuées dans le monde. La plupart de ces moustiquaires sont imprégnées d'insecticides d'une seule et même classe : les pyréthrinoïdes. Pour surmonter la résistance croissante des moustiques aux insecticides, l'OMS recommande d'utiliser des moustiquaires imprégnées de pyréthrinoïde et de PBO ainsi que des moustiquaires à double substance active, qui offrent une meilleure protection contre le paludisme que les moustiquaires standard imprégnées uniquement de pyréthrinoïdes.
À ce jour, plus de 3 milliards de moustiquaires imprégnées d'insecticide ont été distribuées dans le monde. La plupart de ces moustiquaires sont imprégnées d'insecticides d'une seule et même classe : les pyréthrinoïdes. Pour surmonter la résistance croissante des moustiques aux insecticides, l'OMS recommande d'utiliser des moustiquaires imprégnées de pyréthrinoïde et de PBO ainsi que des moustiquaires à double substance active, qui offrent une meilleure protection contre le paludisme que les moustiquaires standard imprégnées uniquement de pyréthrinoïdes.
En 2023, ces moustiquaires à l'efficacité renforcée ont représenté 78 % des 195 millions de moustiquaires livrées en Afrique subsaharienne, soit une augmentation considérable par rapport aux 59 % de 2022.
L'accès plus large à la chimioprévention du paludisme saisonnier est un autre point très positif dans les efforts de lutte contre le paludisme en Afrique
Entre 2012 et 2023, le nombre moyen d'enfants africains traités par cycle de CPS est passé de 170 000 à 53 millions en 2023. En 2023, la CPS a été mise en œuvre dans 19 pays africains, le Nigéria traitant à lui seul 28,6 millions d'enfants. Deux pays ont introduit la CPS pour la première fois en 2023 : la Côte d'Ivoire et Madagascar.
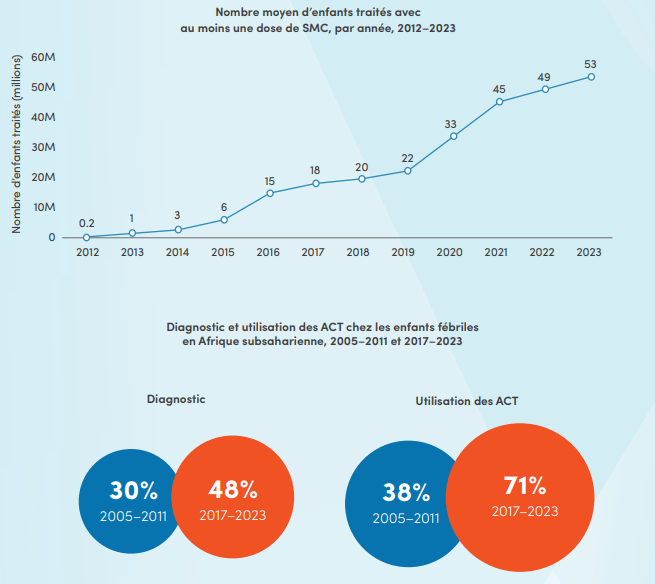 La prise en charge des cas parmi les enfants de moins de cinq ans s'est améliorée
La prise en charge des cas parmi les enfants de moins de cinq ans s'est améliorée
Dans 26 pays d'Afrique subsaharienne, le pourcentage d'enfants avec de la fièvre présentés à un prestataire de santé et pour qui un diagnostic a été établi est passé d'une médiane de 30 % dans les études de référence (de 2005 à 2011) à 48 % dans les enquêtes les plus récentes (de 2017 à 2023). Sur tous les enfants présentés à un prestataire de santé et ayant reçu un médicament antipaludique, une médiane de 71 % a été traitée par ACT de 2017 à 2023, contre 38 % entre 2005 et 2011.
Les ACT représentent le traitement largement préconisé et le plus efficace contre le paludisme sans complication, notamment pour les infections à Plasmodium falciparum, le parasite responsable de la plupart des décès dus au paludisme en Afrique. Voir l'infographie

Masquer l'infographie
Les efforts visant à faciliter l'accès au traitement préventif intermittent pendant la grossesse (TPIp) doivent s'accélérer
Le traitement préventif intermittent pendant la grossesse (TPIp) sert à prévenir le paludisme chez les jeunes filles et femmes enceintes vivant dans des zones de transmission modérée à élevée. L'OMS recommande au moins trois doses de TPIp, avec une première dose le plus tôt possible durant le deuxième trimestre de grossesse. À ce jour, 34 pays d'Afrique ont adopté le TPIp.
4. Quels sont les besoins à ce jour ?
L'atteinte des objectifs fixés au niveau mondial contre le paludisme nécessitera une accélération des mesures d'urgence, surtout dans les pays d'Afrique les plus durement touchés. Les pays d'endémie palustre devraient être soutenus par un écosystème efficace de partenaires internationaux. Le cadre du « Big Push » a pour but de redynamiser la lutte contre le paludisme au niveau mondial en faisant davantage converger le soutien international vers les besoins spécifiques des pays affectés.
La réalisation des objectifs de la Stratégie mondiale exigera plus de ressources et de mesures dans les pays d'Afrique où le paludisme sévit le plus
Au début de cette année, les ministres de la Santé de 11 pays d'Afrique fortement touchés se sont engagés à respecter le principe selon lequel « personne ne devrait mourir du paludisme » compte tenu des ressources et des outils disponibles. En signant la Déclaration de Yaoundé en mars 2024, ils se sont par ailleurs engagés en faveur de sept actions clés ayant pour but d'accélérer les progrès contre le paludisme. Les responsables politiques doivent maintenant traduire les engagements qu'ils ont pris en ressources et en actions concrètes qui sauveront des vies.
Sept actions clés
- Renforcer la volonté politique ;
- Assurer l'utilisation de l'information à des fins stratégiques ;
- Fournir de meilleures techniques d'orientation ;
- Renforcer la coordination et l'action multisectorielle ;
- Renforcer les systèmes de santé nationaux ;
- Établir des partenariats fondés sur la collaboration pour la mobilisation des ressources, la recherche et l'innovation ;
- Garantir l'existence d'un mécanisme efficace de responsabilisation concernant le paludisme.
Actions prioritaires au cours des prochaines cinq années
- Améliorer la coordination entre les partenaires mondiaux, régionaux et nationaux ;
- Soutenir le leadership et la responsabilité au niveau national tout en promouvant une approche inclusive de l'ensemble de la société ;
- Renforcer les systèmes de données et permettre une prise de décision fondée sur les données ;
- Améliorer l'accessibilité, l'acceptabilité et la qualité des interventions existantes ;
- Développer et se préparer à l'introduction rapide de nouveaux outils de transformation :
- Augmenter le financement de la lutte contre le paludisme en s'appuyant sur une nouvelle perspective.
Au sommaire la semaine prochaine :
5. L'accent sur l'équité
Pour la première fois cette année, le rapport sur le paludisme dans le monde comporte un chapitre exclusivement consacré au besoin d'une riposte plus efficace et plus inclusive, mettant l'accent sur l'action auprès des groupes les plus vulnérables face au paludisme et à ses conséquences. Accélérer les progrès en vue d'atteindre les objectifs fixés au niveau mondial exigera une plus grande concertation afin d'identifier et de franchir les obstacles à l'égalité des genres, aux droits humains et à l'équité en santé dans le cadre de la lutte contre le paludisme dans le monde.
Les informations présentées ci-dessus sont extraites de ce document que nous vous invitons à consulter dans son intégralité : Dossier d'information - Principaux messages - Rapport 2024 sur le paludisme dans le monde - 11 décembre 2024 - OMS
Pour aller plus loin, nous vous proposons de consulter ces documents :

Strimol® extra
1. Dénomination du médicament
Strimol extra® comprimé.
2. Composition qualitative et quantitative
Chaque comprimé contient :
- Paracétamol USP : 500 mg ;
- Caféine anhydre USP : 30 mg.
Pour la liste complète des excipients, voir rubrique 6.1.
3 - Forme pharmaceutique
Comprimés blancs à blanc cassé, circulaires, plats, à bords biseautés, avec STRIMOL EXTRA en creux sur une face et en clair sur l'autre.
4. Données cliniques
4.1 Indications thérapeutiques
Contient du paracétamol, qui est un analgésique et un antipyrétique, et de la caféine, un adjuvant de l'effet analgésique du paracétamol.
Traitement symptomatique des douleurs légères à modérées et soulagement de la fièvre, y compris :
- maux de tête ;
- migraine ;
- douleurs musculaires ;.
- dysménorrhée. ;
- maux de gorge ;
- douleurs musculosquelettiques. ;
- fièvre et douleur après une vaccination. ;
- douleur après une intervention dentaire / extraction dentaire ;
- maux de dents. ;
- douleurs de l'arthrose.
Rhume et grippe
Pour le soulagement des symptômes du rhume et de la grippe, par exemple maux de tête, fièvre, maux de gorge, douleurs musculaires, réduction de la vigilance et somnolence.
4.2. Posologie et mode d'administration
Posologie
Adultes et adolescents (>50 kg)
1 à 2 comprimés à laisser dissoudre dans l'eau avant de boire. Cette dose peut être répétée toutes les quatre heures si nécessaire. Maximum quatre doses en 24 heures. Ne pas dépasser la dose indiquée.
Population pédiatrique
Strimol extra n'est pas recommandé pour les enfants de moins de 12 ans.
Insuffisance rénale
Les patients chez qui une insuffisance rénale a été diagnostiquée doivent demander un avis médical avant de prendre ce médicament. Les restrictions liées à l'utilisation de produits à base de paracétamol et de caféine chez les patients atteints d'insuffisance rénale sont principalement une conséquence de la teneur en paracétamol du médicament. (voir rubrique Mises en garde et précautions d'emploi).
Fonction hépatique altérée
Les patients chez qui une insuffisance hépatique a été diagnostiquée doivent demander un avis médical avant de prendre ce médicament. Les restrictions liées à l'utilisation de produits à base de paracétamol et de caféine chez les patients atteints d'insuffisance hépatique sont principalement une conséquence de la teneur en paracétamol de ces médicaments. (voir rubrique Mises en garde et précautions d'emploi).
Mode d'administration
Voie orale.
Les comprimés sont à avaler tels quels avec de l'eau.
4.3. Contre-indications
Strimol extra est contre-indiqué chez les patients ayant des antécédents d'hypersensibilité au paracétamol (caféine ou excipients).
4.4. Mises en garde et précautions d'emploi
- Ne pas utiliser avec d'autres produits contenant du paracétamol. L'utilisation concomitante avec d'autres produits contenant du paracétamol peut entraîner un surdosage. Un surdosage en paracétamol peut entraîner une insuffisance hépatique pouvant conduire à une transplantation du foie ou au décès ;
- Une maladie hépatique sous-jacente augmente le risque de lésions hépatiques liées au paracétamol. Les patients chez qui on a diagnostiqué une insuffisance hépatique ou rénale doivent demander un avis médical avant de prendre ce médicament ;
- Des cas de dysfonctionnement/défaillance hépatique ont été rapportés chez des patients présentant des niveaux de glutathion appauvris, tels que ceux souffrant de malnutrition sévère, d'anorexie, ayant un faible indice de masse corporelle ou étant de gros consommateurs chroniques d'alcool. Chez les patients présentant des états de déplétion en glutathion tels que la septicémie, l'utilisation de paracétamol peut augmenter le risque d'acidose métabolique ;
- Si les symptômes persistent, un avis médical doit être demandé. (Si les symptômes du rhume et de la grippe persistent pendant plus de 7 jours, un avis médical doit être demandé*). ;
- La consommation excessive de caféine (par exemple le café, le thé et certaines boissons en boîte) doit être évitée pendant la prise de ce produit.
- Tenir hors de la vue et de la portée des enfants.
4.5. Interactions avec d'autres médicaments et autres formes d'interactions
Liées à la caféine :
- La phénylpropanolamine augmente les concentrations plasmatiques de caféine de quatre fois. Un risque d'effets indésirables sur le SNC est possible. Des rapports isolés décrivent le développement d'une psychose aiguë lorsque la caféine est administrée avec de la phénylpropanolamine ;
- La fluvoxamine, un inhibiteur puissant du CYP 1 A2, réduit nettement la clairance de la caféine. L'administration concomitante peut entraîner une intoxication à la caféine ;
- La ciprofloxacine réduit le métabolisme de la caféine, entraînant une augmentation de deux fois des concentrations plasmatiques de caféine.
Utiliser avec précaution
- + Norfloxacine : augmentation de la concentration plasmatique de caféine due à l'inhibition de son métabolisme hépatique par la norfloxacine ;
- La caféine, un stimulant du SNC, a un effet antagoniste sur l'action des sédatifs et des tranquillisants. La caféine peut augmenter l'effet tachycardisant de la phénylpropanolamine et d'autres médicaments sympathomimétiques ;
- La caféine peut augmenter la tension artérielle et contrer l'action hypotensive des bêta-bloquants tels que l'aténolol, le métoprolol, l'oxprénolol et le propranolol. Ce médicament ne doit pas être utilisé en même temps que les bêtabloquants ;
- Le disulfirame diminue la clairance de la caféine jusqu'à 50 %. L'utilisation concomitante de disulfirame et de Strimol extra doit être évitée ;
- + Dipyridamole : dipyridamole injectable : diminution de l'effet vasodilatateur du dipyridamole ;
- Le traitement par la caféine doit être interrompu au moins 5 jours avant l'imagerie myocardique. La consommation de café, de thé et de chocolat doit être évitée dans les 24 heures précédant le test ;
- + Enoxacine : augmentation des concentrations plasmatiques de caféine due à une diminution de son métabolisme hépatique pouvant entraîner une excitation ou des hallucinations. L'utilisation concomitante n'est ainsi pas recommandée ;
- + Mexilétine : augmentation de la concentration plasmatique de caféine due à l'inhibition de son métabolisme hépatique par la mexilétine.
Associations à prendre en compte
+Stiripentol : augmentation possible de la concentration plasmatique de caféine avec risque de surdosage, en raison de son inhibition du métabolisme hépatique.
Utiliser avec précaution
- La caféine exerce une inhibition compétitive du métabolisme de la clozapine. Par conséquent, la clozapine et la caféine ne doivent pas être utilisées simultanément ;
- L'utilisation de carbonate de lithium et de caféine peut entraîner une légère diminution des taux sériques de lithium. Par conséquent, l'ingestion concomitante de caféine doit être évitée. En cas d'utilisation concomitante, le risque d'augmentation du lithium sérique lors de l'arrêt brutal de la caféine doit être pris en compte ;
- Les inhibiteurs de la monoamine oxydase peuvent augmenter les effets stimulants de la caféine. ;
- Le methoxsalen réduit la clairance de la caféine et peut augmenter les effets de la caféine. ;
- La phénytoïne double la clairance de la caféine, bien que la caféine n'affecte pas le métabolisme de la phénytoïne. ;
- L'acide pipémidique réduit la clairance de la caféine, améliorant ainsi les effets de la caféine. ;
- La théophylline et la caféine partagent la même voie métabolique, ce qui entraîne une diminution des temps de clairance de la théophylline lorsqu'elle est utilisée en même temps que la caféine. L'utilisation concomitante doit être évitée ;
- La lévothyroxine, comme la caféine peut augmenter la pression artérielle, et donc ces deux substances actives ne doivent pas être utilisées en même temps ;
- L'éphédrine et la caféine interagissent pour produire des effets cardiovasculaires significatifs. Par conséquent, la caféine doit être évitée lors de la prise d'éphédrine.
Liées au paracétamol :
- Les substances hépatotoxiques peuvent augmenter la possibilité d'accumulation de paracétamol et de surdosage. Le risque d'hépatotoxicité du paracétamol peut être augmenté par des médicaments qui induisent des enzymes microsomiques hépatiques telles que les barbituriques, les antidépresseurs tricycliques et l'alcool ;
- Le probénécide diminue presque par deux la clairance du paracétamol en inhibant sa conjugaison avec l'acide glucuronidique. Une réduction de la dose de paracétamol doit être envisagée en cas de traitement concomitant par le probénécide ;
- Le salicylamide peut prolonger la demi-vie d'élimination du paracétamol ;
- Le métoclopramide et la dompéridone accélèrent l'absorption du paracétamol ;
- La cholestyramine réduit l'absorption du paracétamol ;
- Le paracétamol peut affecter la pharmacocinétique du chloramphénicol. Il est recommandé de surveiller les taux plasmatiques de chloramphénicol en combinant le paracétamol avec un traitement par injection de chloramphénicol ;
- L'utilisation concomitante de paracétamol (4 g par jour pendant au moins 4 jours) avec des anti-coagulants oraux peut entraîner de légères variations des valeurs de l'INR. Dans ce cas, une surveillance accrue des valeurs de l'INR doit être effectuée pendant la durée de la combinaison et après son arrêt.
Interférence avec les tests de laboratoire
- Le paracétamol peut affecter les tests d'acide urique par l'acide phospho-wolframique, et les tests de glycémie par la glucose-oxydase-peroxydase ;
- L'isoniazide réduit la clairance du paracétamol de 20 %, avec une potentialisation possible de son action et/ou de sa toxicité, en inhibant son métabolisme dans le foie. La pertinence clinique est inconnue ;
- Le paracétamol diminue la biodisponibilité de la lamotrigine avec une réduction possible de son effet en raison de l'induction possible de son métabolisme dans le foie ;
- L'administration concomitante de paracétamol et de zidovudine peut entraîner une neutropénie ou une hépatotoxicité. Cependant, ces effets n'ont pas été systématiquement signalés. L'utilisation du paracétamol en doses multiples/chroniques chez les patients sous zidovudine doit être évitée ; toutefois, si le paracétamol et la zidovudine doivent être administrés en concomitance, une numération leucocytaire et des tests de la fonction hépatique doivent être effectués, en particulier chez les patients malnutris ;
- La prudence est recommandée lorsque le paracétamol est administré de façon concomitante avec la flucloxacilline en raison du risque accru d'acidose métabolique à trou anionique élevé (AMTAE), en particulier chez les patients présentant un facteur de risque de déficit en glutathion tel qu'une insuffisance rénale sévère, un sepsis, une malnutrition ou un alcoolisme chronique. Une surveillance étroite est recommandée afin de détecter l'apparition de AMTAE, par la recherche de la 5-oxoproline urinaire.
4.6. Grossesse et allaitement
Grossesse
Paracétamol
Les études humaines et animales sur le paracétamol n'ont pas identifié de risque pour la grossesse ou le développement embryonnaire et fœtal.
Caféine
L'utilisation de Strimol extra n'est pas recommandée pendant la grossesse en raison de l'augmentation possible du risque d'avortement spontané associé à la consommation de caféine.
Allaitement
Le paracétamol et la caféine sont excrétés dans le lait maternel.
Paracétamol
Les études menées chez l'homme avec le paracétamol aux doses recommandées n'ont pas identifié de risque pour l'allaitement ou la progéniture allaitée.
Caféine
La caféine présente dans le lait maternel peut potentiellement avoir un effet stimulant sur les enfants nourris au sein, mais aucune toxicité significative n'a été observée.
Fertilité
Il n'y a pas de données disponibles concernant l'influence de Strimol extra sur la fertilité humaine.
4.7. Effets sur l'aptitude à conduire des véhicules et à utiliser des machines
Strimol extra n'a aucun effet ou qu'un effet négligeable sur l'aptitude à conduire des véhicules et à utiliser des machines.
4.8 Effets indésirables
Données post- commercialisation
Les événements rapportés dans le cadre d'une vaste expérience post-commercialisation à la dose thérapeutique/étiquetée et considérés comme attribuables sont présentés ci-dessous par classe de systèmes d'organes et par fréquence.
Les fréquences sont définies comme : très fréquent (> 1/10), fréquent (> 1/100, < 1/10), peu fréquent (> 1/1000, <1/100), rare (> 1/10 000, < 1/1 000), très rare (< 1/10 000 y compris les rapports isolés) et fréquence indéterminée (ne peut être estimée sur la base des données disponibles).
La fréquence des effets indésirables a été estimée à partir des rapports spontanés reçus par le biais des données post- commercialisation.
Classes d'organes |
Effet indésirable |
Fréquence |
Paracétamol |
Troubles du système sanguin et lymphatique |
Thrombocytopénie |
Très rare |
Troubles du système immunitaire |
Anaphylaxie
Réactions d'hypersensibilité cutanée comprenant, entre autres, des éruptions cutanées, un angiodème, le syndrome
de Stevens Johnson. |
Très rare |
Troubles respiratoires, thoraciques et médiastinaux |
Bronchospasme chez les patients sensibles à l'aspirine et aux autres AINS. |
Très rare |
Troubles hépatobiliaires |
Dysfonctionnement hépatique |
Très rare |
Caféine |
Système nerveux central |
Nervosité, vertiges |
Très rare |
Lorsque le schéma posologique recommandé de paracétamol-caféine est associé à un apport alimentaire en caféine, la dose plus élevée de caféine qui en résulte peut augmenter le potentiel d'effets indésirables liés à la caféine tels que l'insomnie, l'agitation, l'anxiété, l'irritabilité, les maux de tête, les troubles gastro-intestinaux et les palpitations. |
Déclaration des effets indésirables suspectés
Vous pouvez signaler les effets secondaires en vous rendant sur le site https://www.strides.com/contact_DS.aspx ou en nous envoyant un courriel à : drugsafety@strides.com.
En signalant les effets indésirables, vous contribuez à fournir davantage d'informations sur la sécurité du médicament.
4.9. Surdosage
Paracétamol
Facteurs de risque
- Si le patient est soumis à un traitement à long terme avec la carbamazépine, le phénobarbitone, la phénytoïne, la primidone, la rifampicine, le millepertuis ou d'autres médicaments qui induisent des enzymes de foie.
- Si le patient consomme régulièrement de l'éthanol au-delà des quantités recommandées.
- Si le patient est susceptible de présenter une diminution en glutathion par exemple : troubles de l'alimentation, fibrose kystique, infection par le VIH, dénutrition, cachexie.
Symptômes
Les symptômes du surdosage de paracétamol dans les premières 24 heures sont la pâleur, les nausées, les vomissements, l'anorexie et les douleurs abdominales. Les lésions hépatiques peuvent apparaître de 12 à 48 heures après l'ingestion. Des anomalies du métabolisme du glucose et de l'acidose métabolique peuvent survenir. En cas d'intoxication sévère, l'insuffisance hépatique peut évoluer vers une encéphalopathie, une hémorragie, une hypoglycémie, un œdème cérébral et la mort.
L'insuffisance rénale aiguë avec nécrose aiguë des tubules rénaux, fortement suggérée par une douleur dorsale, l'hématurie et la protéinurie, peut se développer même en l'absence de lésions hépatiques sévères. Des arythmies cardiaques et une pancréatite ont été rapportées.
Traitement
Un traitement immédiat est essentiel dans la gestion du surdosage de paracétamol. En dépit d'un manque de symptômes précoces significatifs, les patients doivent être immédiatement envoyés à l'hôpital pour des soins médicaux immédiats. Les symptômes peuvent se limiter à des nausées ou des vomissements et ne pas refléter la gravité d'un surdosage ou le risque de lésion d'un organe. La prise en charge doit être conforme aux directives de traitement établies.
Un traitement au charbon actif doit être envisagé dans l'heure après le surdosage. La concentration de paracétamol dans le plasma doit être mesurée 4 heures ou plus après l'ingestion (les concentrations antérieures ne sont pas fiables).
Le traitement par N-acétylcystéine peut être utilisé jusqu'à 24 heures après l'ingestion de paracétamol, cependant, l'effet protecteur maximal est obtenu jusqu'à 8 heures après l'ingestion. L'efficacité de l'antidote diminue fortement après cette période. Si nécessaire, le patient doit recevoir de la N-acétylcystéine par voie intraveineuse, conformément au schéma posologique établi.
Si le vomissement n'est pas un problème, la méthionine par voie orale peut constituer une solution de rechange appropriée pour les régions éloignées, à l'extérieur de l'hôpital, pourvu qu'elle soit administrée dans les 10 à 12 heures suivant le surdosage. Il y a peu de preuves que le lavage gastrique sera bénéfique pour un patient chez qui le paracétamol est la seule substance ingérée.
La prise en charge des patients présentant un dysfonctionnement hépatique grave au-delà de 24 h après l'ingestion doit être discutée avec le centre anti-poison ou un service d'hépatologie.
Caféine
Symptômes
Les symptômes courants comprennent l'anxiété, la nervosité, l'agitation, l'insomnie, l'excitation, les contractions musculaires, la confusion, les convulsions. Pour une consommation élevée de caféine, l'hyperglycémie pourrait également apparaître. Les symptômes cardiaques comprennent la tachycardie et l'arythmie cardiaque. Il faut noter que pour que des symptômes cliniquement significatifs de surdosage en caféine apparaissent avec ce médicament, la quantité ingérée serait associée à une toxicité grave liée au paracétamol.
Traitement
Les symptômes de surdosage de caféine sont contrôlés en réduisant ou en arrêtant l'apport en caféine.
Il n'existe pas d'antidote spécifique, mais des mesures de soutien peuvent être utilisées.
Les symptômes du SNC et les convulsions peuvent être traités avec des benzodiazépines ; la tachycardie supraventriculaire peut être contrôlée en utilisant des ß-bloquants tels que le propranolol, administrés par voie intraveineuse.
5. Propriétés pharmacologiques
5.1. Propriétés pharmacodynamiques
Classe pharmacothérapeutique : Autres analgésiques et antipyrétiques-Anilides ; Paracétamol, associations excluant psycholeptiques ; code ATC : N02BE51.
Paracétamol
Analgésique
Le mécanisme de l'action analgésique n'a pas été entièrement déterminé. Le paracétamol pourrait agir principalement en inhibant la synthèse des prostaglandines dans le système nerveux central (SNC) et, à un moindre degré, par une action périphérique en bloquant la génération de l'impulsion douloureuse. L'action périphérique pourrait aussi être due à l'inhibition de la synthèse des prostaglandines ou à l'inhibition de la synthèse ou à des actions d'autres substances sensibilisant les récepteurs de la douleur à la stimulation mécanique ou chimique.
Antipyrétique
L'effet antipyrétique du paracétamol est probablement dû à une action sur le centre hypothalamique thermorégulateur qui entraîne une vasodilatation périphérique responsable d'une augmentation du flux sanguin à travers la peau, d'une sudation et d'une perte de chaleur. L'action centrale implique probablement une inhibition de la synthèse des prostaglandines au sein de l'hypothalamus.
Caféine
Stimulant du système nerveux central
La caféine stimule tous les niveaux du SNC, bien que ses effets corticaux soient plus faibles et de durée plus courte que ceux des amphétamines.
Adjuvant analgésique
La caféine produit une vasoconstriction cérébrale avec une diminution concomitante du débit sanguin cérébral et de la tension d'oxygène du cerveau. Il est suggéré que la caféine aide à soulager les maux de tête en offrant un début d'action plus rapide et/ou un soulagement accru de la douleur avec des doses plus faibles d'analgésique.
5.2. Propriétés pharmacocinétiques
Paracétamol
Absorption
Le paracétamol est facilement absorbé par le tractus gastro-intestinal et est distribué de manière relativement uniforme dans la plupart des fluides corporels, les concentrations plasmatiques maximales étant atteintes environ 30 minutes à 2 heures après l'ingestion.
Distribution
Il est métabolisé dans le foie. Les 2 principales voies métaboliques sont la glucuronidation et la sulfoconjugaison. Cette dernière voie est rapidement saturable avec une posologie supérieure aux doses thérapeutiques. Une voie secondaire, catalysée par le cytochrome P 450, est la formation d'un intermédiaire réactif (N-acétyl benzoquinone imine) qui, dans les conditions normales d'utilisation, est rapidement détoxifié par le glutathion réduit et éliminé dans les urines après sa conjugaison à la cystéine et l'acide mercaptopurique. D'autre part, lors d'intoxications massives, la quantité de ce métabolite toxique est augmentée.
Elimination
Il est excrété dans l'urine principalement sous forme de sulfoconjugués et glycuroconjugués. Une quantité inférieure à 5 % est excrétée sous forme de paracétamol intact. 90 % de la dose ingérée est éliminée par le rein en 24 heures, principalement sous forme conjuguée au glucuronide (60 à 80 %) et sous forme de sulfate conjugué (20 à 30 %). Moins de 5 % est éliminé sous forme inchangée. La demi-vie d'élimination varie d'environ 1 à 4 heures. La liaison plasma-protéine est négligeable aux concentrations thérapeutiques usuelles mais augmente avec des concentrations croissantes.
Un métabolite hydroxylé mineur, généralement produit en très petites quantités par des oxydases à fonction mixte dans le foie et qui est détoxifié par conjugaison avec le glutathion hépatique, peut s'accumuler après un surdosage de paracétamol et provoquer des lésions hépatiques.
Variations physiopathologiques
Insuffisance rénale : En cas d'insuffisance rénale sévère (clairance de la créatinine inférieure à 10 ml / min), l'élimination du paracétamol et de ses métabolites est retardée.
Caféine
Absorption
La caféine est absorbée facilement après l'administration orale et est largement distribuée dans tout le corps. La caféine est presque entièrement métabolisée par oxydation, déméthylation et acétylation.
Distribution
Les concentrations plasmatiques maximales sont atteintes en une heure et la demi-vie plasmatique est d'environ 3,5 heures. 65 à 80 % de la caféine administrée est excrétée dans l'urine sous forme d'acide 1-méthylurique et de 1-méthylxanthine.
Elimination
Elle est excrétée dans l'urine sous forme d'acide 1-méthylurique, de 1-méthylxanthine, de 7-méthylxanthine, de 1,7-diméthylxanthine (paraxanthine), de 5-acétylamino-6-formylamino-3-méthyluracile (AFMU) et d'autres métabolites avec seulement 1 % inchangé.
5.3. Données de sécurité préclinique
Liées au paracétamol
Aucune étude conventionnelle s'appuyant sur les normes actuellement admises pour évaluer la toxicité pour la reproduction et le développement n'est disponible.
Il n'y a pas de données précliniques pertinentes pour le prescripteur en plus de celles déjà couvertes dans d'autres sections du RCP.
6. Données pharmaceutiques
6.1. Liste des excipients
- Amidon de maïs ;
- Silice colloïdale anhydre ;
- Povidone (K-30) ;
- Benzoate de sodium ;
- 4-Hydroxybenzoate de méthyle (méthylparabène) ;
- 4-Hydroxybenzoate de propyle (propylparabène) ;
- Talc purifié ;
- Stéarate de magnésium ;
- Glycolate d'amidon de sodium ;
- Sulfate de lauryle de sodium.
Excipients à effets notoires :
a) Le méthylparabène et le propylparabène peuvent provoquer des réactions allergiques (éventuellement retardées).
b) Le benzoate de sodium peut augmenter la jaunisse (jaunissement de la peau et des yeux) chez les nouveau-nés (jusqu'à 4 semaines).
6.2. Incompatibilités
Sans objet.
6.3. Durée de conservation
36 mois.
6.4. Précautions particulières de conservation
Conserver à une température inférieure à 25°C. Protéger de la lumière. Tenir tous les médicaments hors de portée des enfants.
6.5. Nature et contenu de l'emballage extérieur
Comprimés blancs à blanc cassé, circulaires, plats, à bords biseautés, avec STRIMOL EXTRA en creux sur une face et en clair sur l'autre.
Boîte de 20 comprimés (5 blisters de 4 comprimés).
6.6. Précautions particulières d'élimination et de manipulation
Pas d'exigences particulières.
7. Nom du fabricant
Strides Pharma Science Limited
36/7, Suragajakkanahalli Indlavadi Cross, Anekal Taluk,
Bangalore-562 106, India.
8. Titulaire de l'Autorisation de Mise sur le Marché
Strides Pharma Science Limited
Strides House' Bilekahalli,
Bannerghatta Road,
Bangalore - 560 076, INDIA.
Tel: 91-80-66580738/739
Fax: 91-80-66580700 /800
9. Date de mise à jour du texte
26/06/2023.
Dernière mise à jour de cette page : 01/02/2024
CONDITIONS DE PRESCRIPTION ET DE DELIVRANCE
Médicament non soumis à prescription médicale.

 Identifiez-vous | Inscription
Identifiez-vous | Inscription
 Identifiez-vous | Inscription
Identifiez-vous | Inscription



![]() Adresse
Adresse![]() Téléphone
Téléphone