Rapport 2024 sur le paludisme dans le monde - Principaux messages (Focus Afrique)
Les ripostes au paludisme mises en œuvre dans le monde entier préviennent la maladie et sauvent des vies
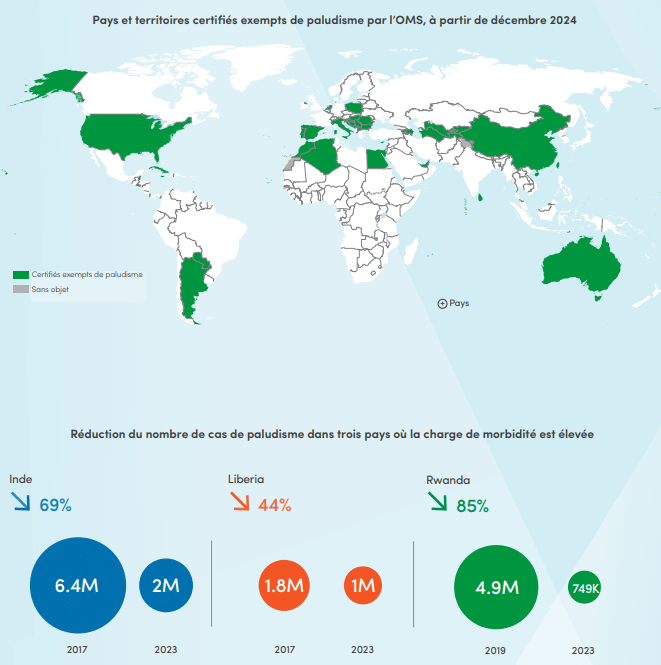 Depuis 2000, les efforts déployés pour lutter contre le paludisme ont permis d'éviter 2,2 milliards de cas et 12,7 millions de décès dans le monde. En plus de diverses interventions ciblées, d'autres facteurs tels que les améliorations des conditions socioéconomiques, ainsi que dans les domaines de la nutrition, des infrastructures, de l'habitat et de l'urbanisation ont vraisemblablement aidé à réduire la transmission et le poids du paludisme.
Depuis 2000, les efforts déployés pour lutter contre le paludisme ont permis d'éviter 2,2 milliards de cas et 12,7 millions de décès dans le monde. En plus de diverses interventions ciblées, d'autres facteurs tels que les améliorations des conditions socioéconomiques, ainsi que dans les domaines de la nutrition, des infrastructures, de l'habitat et de l'urbanisation ont vraisemblablement aidé à réduire la transmission et le poids du paludisme.
Des progrès ont été enregistrés dans de nombreux pays, l'OMS a certifié 44 pays et 1 territoire exempts de paludisme, y compris très récemment l'Égypte et certains pays à charge palustre élevée réalisent également des progrès remarquables :
Dans la région Afrique de l'OMS, le Rwanda a réduit de 85 % son nombre de cas de paludisme entre 2019 et 2023, passant de 4,9 millions de cas estimés à 749 000, alors que le Libéria a enregistré une diminution de 44 % de son nombre de cas depuis 2017, soit une baisse de 1,8 million à 1 million. Dans la région Asie du Sud Est, l'Inde a réduit son nombre de cas de 69 %, avec 6,4 millions de cas en 2017 contre 2 millions en 2023. Voir l'infographie

Masquer l'infographie
Toutefois, le paludisme reste un défi majeur de santé mondiale, surtout dans la région Afrique déjà durement touchée
En 2023, le nombre des nouveaux cas de paludisme estimés a atteint 263 millions dans 83 pays à travers le monde, contre 252 millions en 2022 et 226 millions en 2015. Entre 2022 et 2023, l'Éthiopie (+4,5 millions), Madagascar (+2,7 millions), le Pakistan (+1,6 million), le Nigéria (+1,4 million) et la République démocratique du Congo (+600 000) sont les pays qui ont le plus largement contribué à cette hausse. L'incidence du paludisme, qui est liée à la croissance démographique, a augmenté durant la période 2015–2023, passant de 58 à 60,4 cas pour 1 000 habitants exposés au risque de paludisme.
Le nombre total de décès dus au paludisme dans le monde s'est élevé à 597 000 en 2023 contre 578 000 en 2015. En 2020, les perturbations causées par la pandémie de COVID-19 ont entraîné une forte hausse des décès associés au paludisme, avec 55 000 morts supplémentaires. Le nombre total de décès a réduit progressivement durant les années postCOVID, tout comme le taux de mortalité.
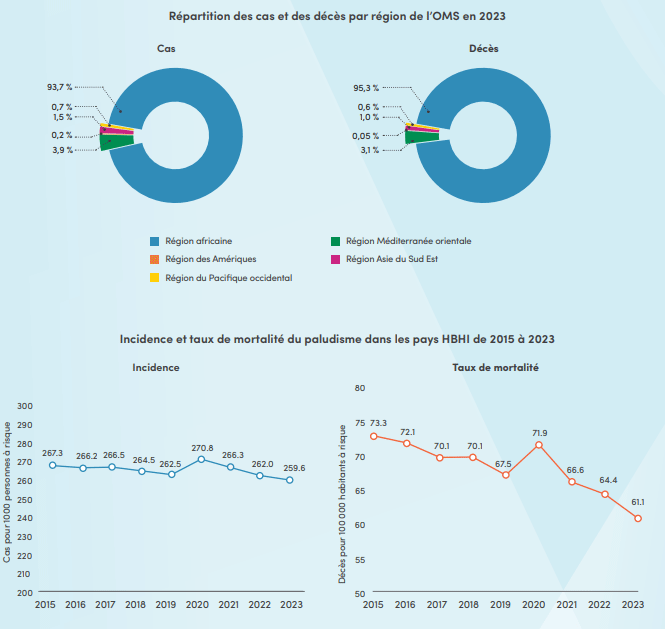
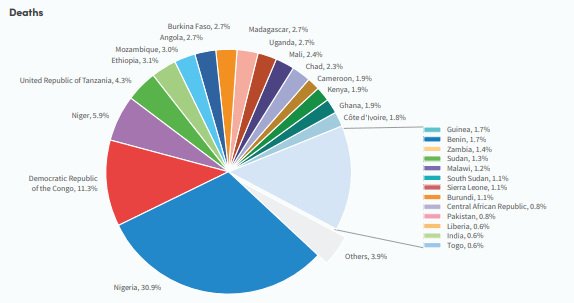
La région Afrique paye toujours le plus lourd tribut, cumulant à elle seule 94 % du nombre total des cas et 95 % des décès associés au paludisme au niveau mondial selon les estimations de 2023. Un peu plus de la moitié de ces décès ont été enregistrés dans quatre pays : Niger (5,9%), Nigéria (30,9%), République démocratique du Congo (11,3%) et République-Unie de Tanzanie (4,3%).
Bien que la riposte au paludisme en Afrique ait remporté quelques succès, il est temps de progresser plus rapidement
 Près des deux tiers des nombres de cas de paludisme et de décès associés au niveau mondial sont concentrés dans 11 pays d'Afrique : Burkina Faso, Cameroun, Ghana, Mali, Mozambique, Niger, Nigéria, Ouganda, Soudan, République démocratique du Congo et République-Unie de Tanzanie. Ces 11 pays ont adopté l'approche « D'une charge élevée à un fort impact » (HBHI), une riposte ciblée ayant pour objet d'atteindre les populations exposées au risque de paludisme le plus élevé grâce à des ensembles d'interventions adaptés sur mesure, tenant compte des données locales et des conditions spécifiques.
Près des deux tiers des nombres de cas de paludisme et de décès associés au niveau mondial sont concentrés dans 11 pays d'Afrique : Burkina Faso, Cameroun, Ghana, Mali, Mozambique, Niger, Nigéria, Ouganda, Soudan, République démocratique du Congo et République-Unie de Tanzanie. Ces 11 pays ont adopté l'approche « D'une charge élevée à un fort impact » (HBHI), une riposte ciblée ayant pour objet d'atteindre les populations exposées au risque de paludisme le plus élevé grâce à des ensembles d'interventions adaptés sur mesure, tenant compte des données locales et des conditions spécifiques.
L'incidence de la maladie (cas pour 1 000 habitants exposés au risque de paludisme) et les taux de mortalité (décès pour 100 000 habitants exposés au risque de paludisme) dans les 11 pays HBHI ont respectivement reculé de 3 % et 13 % entre 2017 et 2023.
De 2015 à 2023, la région Afrique dans son ensemble a réussi à réduire de 5 % l'incidence de la maladie et de 16 % les taux de mortalité. Toutefois, les chiffres de 2023 pour ces deux indicateurs équivalaient encore à plus du double des cibles fixées par la Stratégie mondiale. Voir l'infographie

Masquer l'infographie
2. Principales menaces pesant sur les progrès Voir le chapitre 2
 Au lendemain de la pandémie de COVID-19, les pays d'endémie palustre font face à des défis persistants. La fragilité des systèmes de santé, l'insuffisance de la surveillance et le manque chronique de fonds demeurent des obstacles majeurs.
Au lendemain de la pandémie de COVID-19, les pays d'endémie palustre font face à des défis persistants. La fragilité des systèmes de santé, l'insuffisance de la surveillance et le manque chronique de fonds demeurent des obstacles majeurs.
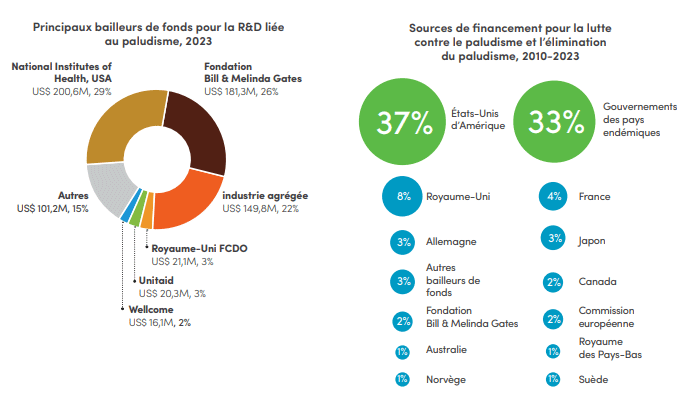
En 2023, les fonds disponibles sont restés nettement inférieurs à l'objectif de US$ 8,3 milliards
Au niveau mondial, les investissements dans la lutte contre le paludisme ont totalisé, selon les estimations, US$ 4 milliards en 2023, un chiffre bien en-deçà de l'objectif de US$ 8,3 milliards fixé dans la Stratégie mondiale de lutte contre le paludisme. Le déficit de financement s'est accentué ces cinq dernières années, passant de US$ 2,6 milliards en 2019 à US$ 4,3 milliards en 2023. Voir l'infographie

Masquer l'infographie
Les urgences humanitaires augmentent les risques de paludisme dans de nombreux pays endémiques
En Éthiopie, le nombre de cas de paludisme estimés a également plus que triplé, passant de 2,6 millions en 2019 à 9,5 millions en 2023. Ces dernières années, les services de santé de base et les mesures de prévention du paludisme ont été perturbés dans les zones de conflit et le pays a dû faire face à d'autres défis, y compris l'émergence du moustique Anopheles stephensi, la résistance aux insecticides et les effets du changement climatique.
Le changement climatique menace les avancées réalisées dans la lutte contre le paludisme
Les températures en hausse et l'évolution des phénomènes météorologiques nuisent à la santé, à la sécurité et aux moyens de subsistance des populations dans le monde entier. Les premières victimes des effets les plus graves du changement climatique sont les communautés vulnérables en Afrique et plusieurs d'entre elles sont déjà plus exposées au risque de contracter le paludisme.
De nombreuses populations exposées au risque de paludisme n'ont toujours pas accès aux services essentiels de prévention, diagnostic et traitement du paludisme
En 2023 par exemple, plus de 40 % des enfants de moins de cinq ans ainsi que des jeunes filles et femmes enceintes en Afrique subsaharienne n'ont pas dormi sous une moustiquaire imprégnée d'insecticide, qui est portant un outil essentiel de prévention du paludisme.
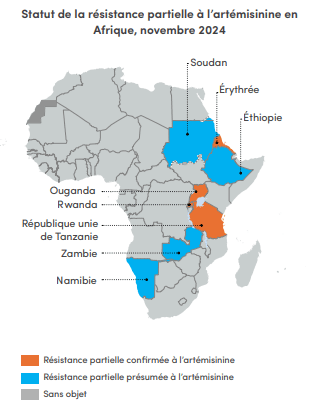 En Afrique, la propagation de la résistance aux médicaments antipaludiques est une vive source d'inquiétude
En Afrique, la propagation de la résistance aux médicaments antipaludiques est une vive source d'inquiétude
À ce jour, quatre pays d'Afrique de l'Est confirment la présence d'une résistance partielle à l'artémisinine (Érythrée, Ouganda, RépubliqueUnie de Tanzanie et Rwanda). En se basant sur les données disponibles, la même résistance est également suspectée dans quatre autres pays (Éthiopie, Namibie, Soudan et Zambie).
En 2022, l'OMS a lancé une stratégie visant à freiner la résistance aux antipaludiques en Afrique. Cette stratégie s'appuie sur les leçons tirées des plans d'action mondiaux du passé et complète les stratégies existantes, en y incluant des efforts plus intenses pour faire face à la résistance antimicrobienne.
Les quatre piliers de la « Stratégie de riposte face à la résistance aux antipaludiques en Afrique » :
- Renforcer la surveillance de la résistance aux antipaludiques et de leur efficacité ;
- Optimiser et mieux réglementer l'usage des produits de diagnostic et des moyens thérapeutiques pour limiter la pression médicamenteuse en prenant des mesures préemptives ;
- Réagir à la résistance en limitant la propagation des parasites résistant aux antipaludiques ;
- Stimuler la recherche et l'innovation afin de mieux exploiter les outils existants et mettre au point de nouveaux outils contre la résistance.
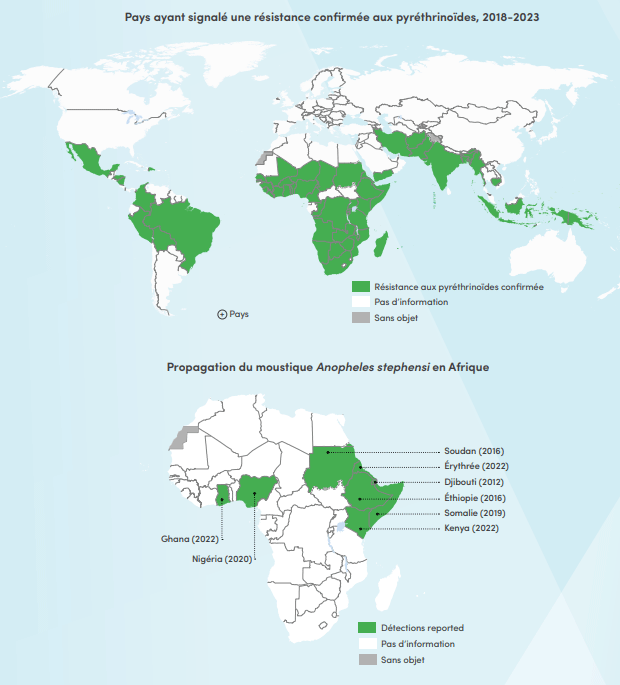 La résistance des moustiques aux pyréthrinoïdes reste très répandue
La résistance des moustiques aux pyréthrinoïdes reste très répandue
La résistance aux pyréthrinoïdes, le produit chimique le plus couramment utilisé sur les moustiquaires imprégnées d'insecticide, a été confirmée dans 55 des 64 pays où elle a été surveillée de 2018 à 2023. Les moustiquaires de nouvelle génération, qui offrent une meilleure protection contre le paludisme que les moustiquaires imprégnées uniquement de pyréthrinoïdes, sont de plus en plus souvent disponibles et constituent un outil important intégré aux efforts de lutte contre le paludisme à l'échelle mondiale. L'OMS a publié des recommandations concernant leur utilisation en 2017 et 2023, respectivement.
Le moustique Anopheles stephensi présente un défi supplémentaire pour la lutte contre le paludisme en Afrique
Originaires d'Asie du Sud et de la péninsule arabique, les espèces de moustiques invasives se sont répandues au cours de la dernière décennie et ont été détectées dans huit pays d'Afrique. An. stephensi peut se développer en milieux urbains, résiste à de fortes températures ainsi qu'à de nombreux insecticides utilisés dans le domaine de la santé publique. En 2022, l'OMS a lancé une initiative [en anglais uniquement] dans le but de sensibiliser ses États membres et partenaires à cette menace croissante et de catalyser les efforts déjà déployés pour stopper la propagation d'An. stephensi en Afrique. Voir l'infographie

Masquer l'infographie
3. Quels sont les progrès accomplis ? Voir le chapitre 3
Le rapport 2024 met en avant les tendances positives enregistrées concernant l'intensification des outils de prévention efficaces, notamment les moustiquaires de nouvelle génération, les vaccins contre le paludisme et la chimioprévention du paludisme saisonnier.
Des progrès significatifs ont également été réalisés dans le domaine des services précoces de diagnostic et de traitement auprès des jeunes enfants. Toutefois, la couverture des moustiquaires imprégnées d'insecticide (MII) et des traitements préventifs du paludisme chez les jeunes filles et femmes enceintes accuse toujours du retard et les zones affichant les chiffres les plus bas nécessitent des mesures complémentaires.
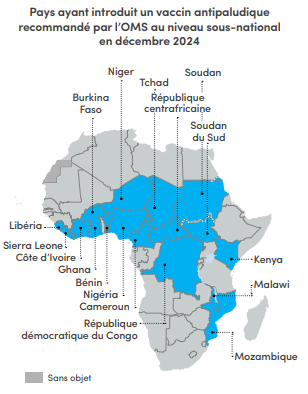 Le déploiement plus important des vaccins promet également d'alléger le fardeau de la maladie en Afrique
Le déploiement plus important des vaccins promet également d'alléger le fardeau de la maladie en Afrique
L'utilisation de deux vaccins antipaludiques, RTS,S/AS01 (RTS,S) et R21/Matrix-M, est désormais recommandée par l'OMS dans les zones d'endémie palustre. De 2019 à 2023, près de 2 millions d'enfants au Ghana, au Kenya et au Malawi ont été vaccinés avec RTS,S. Une évaluation de l'impact a révélé une réduction de 13 % du taux de mortalité toutes causes confondues (à l'exclusion des blessures) et de 22 % des hospitalisations pour paludisme grave chez des enfants admissibles en âge à la vaccination durant cette période.
L'intensification de la vaccination antipaludique en Afrique devrait sauver des dizaines de milliers de jeunes vies chaque année. L'impact maximal sera atteint dès que les vaccins seront administrés parallèlement à une combinaison d'autres interventions de lutte contre le paludisme recommandées par l'OMS et adaptées aux conditions locales.
Le déploiement des moustiquaires de nouvelle génération a grandement progressé ces dernières années
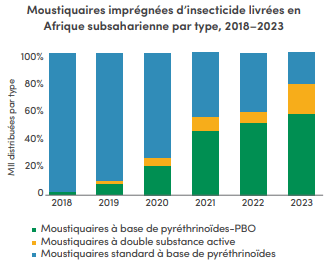 À ce jour, plus de 3 milliards de moustiquaires imprégnées d'insecticide ont été distribuées dans le monde. La plupart de ces moustiquaires sont imprégnées d'insecticides d'une seule et même classe : les pyréthrinoïdes. Pour surmonter la résistance croissante des moustiques aux insecticides, l'OMS recommande d'utiliser des moustiquaires imprégnées de pyréthrinoïde et de PBO ainsi que des moustiquaires à double substance active, qui offrent une meilleure protection contre le paludisme que les moustiquaires standard imprégnées uniquement de pyréthrinoïdes.
À ce jour, plus de 3 milliards de moustiquaires imprégnées d'insecticide ont été distribuées dans le monde. La plupart de ces moustiquaires sont imprégnées d'insecticides d'une seule et même classe : les pyréthrinoïdes. Pour surmonter la résistance croissante des moustiques aux insecticides, l'OMS recommande d'utiliser des moustiquaires imprégnées de pyréthrinoïde et de PBO ainsi que des moustiquaires à double substance active, qui offrent une meilleure protection contre le paludisme que les moustiquaires standard imprégnées uniquement de pyréthrinoïdes.
En 2023, ces moustiquaires à l'efficacité renforcée ont représenté 78 % des 195 millions de moustiquaires livrées en Afrique subsaharienne, soit une augmentation considérable par rapport aux 59 % de 2022.
L'accès plus large à la chimioprévention du paludisme saisonnier est un autre point très positif dans les efforts de lutte contre le paludisme en Afrique
Entre 2012 et 2023, le nombre moyen d'enfants africains traités par cycle de CPS est passé de 170 000 à 53 millions en 2023. En 2023, la CPS a été mise en œuvre dans 19 pays africains, le Nigéria traitant à lui seul 28,6 millions d'enfants. Deux pays ont introduit la CPS pour la première fois en 2023 : la Côte d'Ivoire et Madagascar.
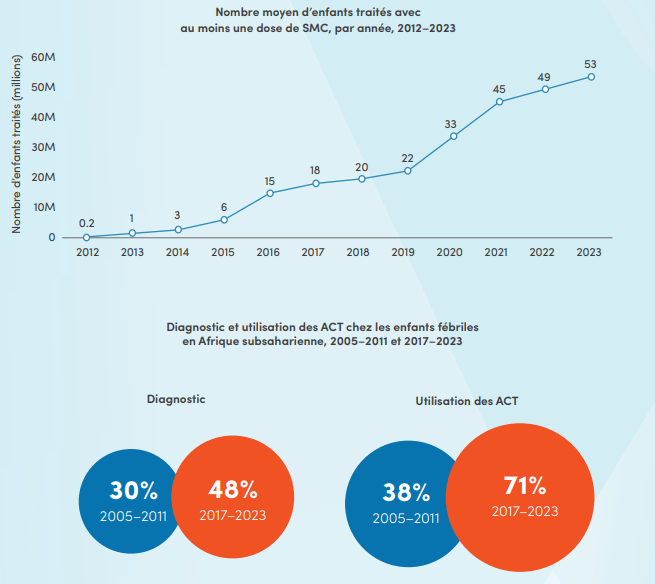 La prise en charge des cas parmi les enfants de moins de cinq ans s'est améliorée
La prise en charge des cas parmi les enfants de moins de cinq ans s'est améliorée
Dans 26 pays d'Afrique subsaharienne, le pourcentage d'enfants avec de la fièvre présentés à un prestataire de santé et pour qui un diagnostic a été établi est passé d'une médiane de 30 % dans les études de référence (de 2005 à 2011) à 48 % dans les enquêtes les plus récentes (de 2017 à 2023). Sur tous les enfants présentés à un prestataire de santé et ayant reçu un médicament antipaludique, une médiane de 71 % a été traitée par ACT de 2017 à 2023, contre 38 % entre 2005 et 2011.
Les ACT représentent le traitement largement préconisé et le plus efficace contre le paludisme sans complication, notamment pour les infections à Plasmodium falciparum, le parasite responsable de la plupart des décès dus au paludisme en Afrique. Voir l'infographie

Masquer l'infographie
Les efforts visant à faciliter l'accès au traitement préventif intermittent pendant la grossesse (TPIp) doivent s'accélérer
Le traitement préventif intermittent pendant la grossesse (TPIp) sert à prévenir le paludisme chez les jeunes filles et femmes enceintes vivant dans des zones de transmission modérée à élevée. L'OMS recommande au moins trois doses de TPIp, avec une première dose le plus tôt possible durant le deuxième trimestre de grossesse. À ce jour, 34 pays d'Afrique ont adopté le TPIp.
4. Quels sont les besoins à ce jour ? Voir le chapitre 4
L'atteinte des objectifs fixés au niveau mondial contre le paludisme nécessitera une accélération des mesures d'urgence, surtout dans les pays d'Afrique les plus durement touchés. Les pays d'endémie palustre devraient être soutenus par un écosystème efficace de partenaires internationaux. Le cadre du « Big Push » a pour but de redynamiser la lutte contre le paludisme au niveau mondial en faisant davantage converger le soutien international vers les besoins spécifiques des pays affectés.
La réalisation des objectifs de la Stratégie mondiale exigera plus de ressources et de mesures dans les pays d'Afrique où le paludisme sévit le plus
Au début de cette année, les ministres de la Santé de 11 pays d'Afrique fortement touchés se sont engagés à respecter le principe selon lequel « personne ne devrait mourir du paludisme » compte tenu des ressources et des outils disponibles. En signant la Déclaration de Yaoundé en mars 2024, ils se sont par ailleurs engagés en faveur de sept actions clés ayant pour but d'accélérer les progrès contre le paludisme. Les responsables politiques doivent maintenant traduire les engagements qu'ils ont pris en ressources et en actions concrètes qui sauveront des vies.
Sept actions clés
- Renforcer la volonté politique ;
- Assurer l'utilisation de l'information à des fins stratégiques ;
- Fournir de meilleures techniques d'orientation ;
- Renforcer la coordination et l'action multisectorielle ;
- Renforcer les systèmes de santé nationaux ;
- Établir des partenariats fondés sur la collaboration pour la mobilisation des ressources, la recherche et l'innovation ;
- Garantir l'existence d'un mécanisme efficace de responsabilisation concernant le paludisme.
Actions prioritaires au cours des prochaines cinq années
- Améliorer la coordination entre les partenaires mondiaux, régionaux et nationaux ;
- Soutenir le leadership et la responsabilité au niveau national tout en promouvant une approche inclusive de l'ensemble de la société ;
- Renforcer les systèmes de données et permettre une prise de décision fondée sur les données ;
- Améliorer l'accessibilité, l'acceptabilité et la qualité des interventions existantes ;
- Développer et se préparer à l'introduction rapide de nouveaux outils de transformation :
- Augmenter le financement de la lutte contre le paludisme en s'appuyant sur une nouvelle perspective.
 Pour la première fois cette année, le rapport sur le paludisme dans le monde comporte un chapitre exclusivement consacré au besoin d'une riposte plus efficace et plus inclusive, mettant l'accent sur l'action auprès des groupes les plus vulnérables face au paludisme et à ses conséquences. Accélérer les progrès en vue d'atteindre les objectifs fixés au niveau mondial exigera une plus grande concertation afin d'identifier et de franchir les obstacles à l'égalité des genres, aux droits humains et à l'équité en santé dans le cadre de la lutte contre le paludisme dans le monde.
Pour la première fois cette année, le rapport sur le paludisme dans le monde comporte un chapitre exclusivement consacré au besoin d'une riposte plus efficace et plus inclusive, mettant l'accent sur l'action auprès des groupes les plus vulnérables face au paludisme et à ses conséquences. Accélérer les progrès en vue d'atteindre les objectifs fixés au niveau mondial exigera une plus grande concertation afin d'identifier et de franchir les obstacles à l'égalité des genres, aux droits humains et à l'équité en santé dans le cadre de la lutte contre le paludisme dans le monde.
Par exemple, la prévalence du paludisme chez les enfants de moins de cinq ans en Afrique subsaharienne atteint des niveaux exagérément élevés au sein des ménages à faible revenu et diminue avec la courbe ascendante du statut économique.
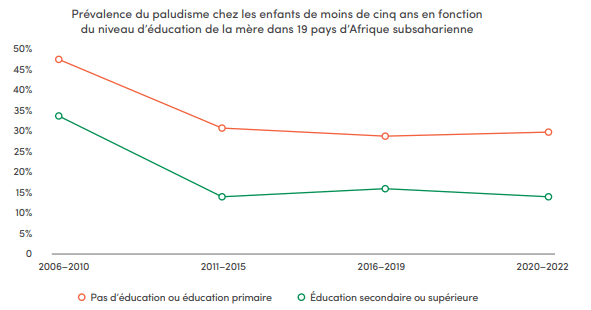
D'autres déterminants peuvent aggraver le risque de paludisme chez un enfant, notamment le niveau d'éducation de sa mère.
- De 2020 à 2022, les enfants de moins de cinq ans dont les mères n'avaient jamais été scolarisées ou qui avaient quitté l'école à la fin de l'enseignement primaire ont eu deux fois plus de risque de contracter le paludisme que les enfants dont les mères avaient atteint le secondaire ou des niveaux d'instruction supérieurs ;
- Les recherches ont démontré une corrélation entre le niveau d'instruction d'une mère et son propre risque de paludisme ;
- Les chances que des jeunes filles et des femmes enceintes ayant atteint un niveau scolaire plus élevé cherchent à obtenir les 3 doses ou plus recommandées de traitement préventif du paludisme et utilisent une moustiquaire imprégnée d'insecticide (MII) sont plus élevées que parmi celles qui n'ont bénéficié que d'un enseignement scolaire limité. Voir l'infographie

Masquer l'infographie
Au-delà des défis à surmonter pour accéder à l'éducation, de nombreuses jeunes filles et femmes doivent franchir d'autres obstacles qui entravent l'amélioration des résultats de la lutte contre le paludisme, mais aussi l'égalité des genres, tels que des connaissances limitées sur le paludisme, des ressources financières insuffisantes et un manque d'influence dans la prise de décisions au sein du ménage.
 Les rôles basés sur le genre qui se reflètent sur le marché du travail et dans les attentes sociales influencent le risque d'exposition à la maladie dans les régions d'endémie palustre.
Les rôles basés sur le genre qui se reflètent sur le marché du travail et dans les attentes sociales influencent le risque d'exposition à la maladie dans les régions d'endémie palustre.
Par exemple, les tâches domestiques souvent assignées aux jeunes filles et aux femmes sont généralement accomplies à l'extérieur, tôt le matin et en soirée, c'est-à-dire au moment des pics d'activité des moustiques, ce qui augmente leur risque de contracter le paludisme.
Dans certaines régions, les garçons et les hommes payent également un tribut disproportionné au paludisme du fait de stéréotypes, de rôles et de relations préjudiciables en matière d'égalité des genres.
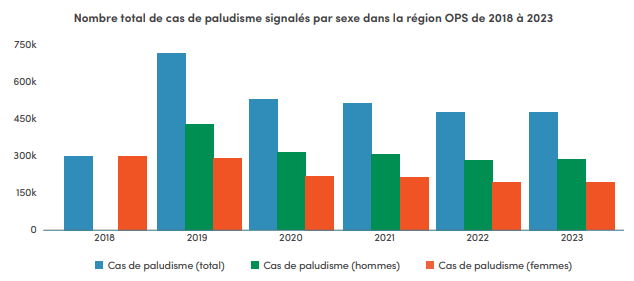
En effet, travailler dans certains secteurs comme l'agriculture, la foresterie, le service militaire et l'exploitation minière, supposent la plupart du temps des environnements propices à la transmission du paludisme, ce qui amplifie l'exposition à la maladie. Dans la région de l'Organisation panaméricaine de la santé (OPS), où l'extraction aurifère contribue largement à la transmission systématique du paludisme, les garçons et les hommes ont enregistré plus de cas de paludisme et de décès associés que les jeunes filles et les femmes entre 2018 et 2023. Voir l'infographie

Masquer l'infographie
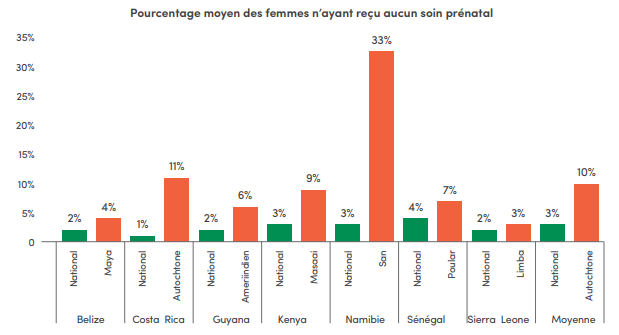 Dans le monde entier, les peuples autochtones affichent habituellement des taux d'invalidité et de maladie plus élevés, rencontrent de plus grandes difficultés pour accéder aux services de santé et bénéficient d'une espérance de vie nettement plus courte que tous les autres citoyens de leur pays. Les adolescentes et les femmes autochtones, par exemple, doivent relever de véritables défis pour accéder à des soins prénatals au niveau mondial. Les femmes autochtones sont souvent privées des traitements préventifs du paludisme, ce qui menace davantage encore leur propre santé et celle de leurs enfants. Voir l'infographie
Dans le monde entier, les peuples autochtones affichent habituellement des taux d'invalidité et de maladie plus élevés, rencontrent de plus grandes difficultés pour accéder aux services de santé et bénéficient d'une espérance de vie nettement plus courte que tous les autres citoyens de leur pays. Les adolescentes et les femmes autochtones, par exemple, doivent relever de véritables défis pour accéder à des soins prénatals au niveau mondial. Les femmes autochtones sont souvent privées des traitements préventifs du paludisme, ce qui menace davantage encore leur propre santé et celle de leurs enfants. Voir l'infographie

Masquer l'infographie
Pour faire face à des vulnérabilités qui s'additionnent, il est impératif d'élaborer des actions et des politiques qui, en plus d'être fondées sur des données factuelles, tiennent compte du genre, intègrent une démarche d'équité et s'appuient sur les principes des droits humains
Pour améliorer les ripostes au paludisme dans le monde et s'assurer qu'elles atteignent les plus vulnérables, les pays et leurs partenaires de développement doivent envisager et mener les politiques suivantes :
S'engager à renforcer les soins de santé primaires (SSP), car ils forment la base de systèmes de santé efficaces, équitables et solides. Pour ce faire :
- Fournir des soins de santé de bonne qualité et abordables, gommant les inégalités de genre et adaptés sur le plan culturel, offrant une protection financière à toutes et tous, y compris les populations à risque et les personnes vivant dans des zones reculées et dans un contexte de crise humanitaire. Les services de santé, dont font partie les interventions antipaludiques, doivent être de bonne qualité, acceptables, accessibles et disponibles pour toutes les personnes en ayant besoin. Ces services doivent également être proches du lieu où les gens vivent et travaillent, en intégrant si nécessaire la contribution des agents de santé communautaires pour fournir des services de santé de base et d'urgence vitale ;
- Encourager la participation active et éclairée des individus et des communautés dans la prise de décisions qui affectent leur santé, en encourageant l'appropriation, la responsabilité et le caractère durable des interventions antipaludiques ;
- Promouvoir une vaste riposte multisectorielle qui s'attaque aux causes profondes du paludisme, en s'articulant autour de la réduction de la pauvreté et des stratégies spécifiques au genre, pour prévenir la maladie, améliorer le bien-être, augmenter la prospérité et la productivité, et alléger les charges qui pèsent sur les systèmes de santé.
S'attaquer aux causes profondes des inégalités fondées sur le genre ainsi qu'aux autres déterminants du paludisme.
Il convient alors de remettre en question les normes existantes liées au genre, les déséquilibres des pouvoirs et les lois discriminatoires pour obtenir un « double dividende », tant au niveau de l'amélioration des résultats de la lutte contre le paludisme que de la réduction des inégalités.
Investir dans de meilleurs systèmes de données :
Pour améliorer les résultats de la lutte contre le paludisme, éliminer les obstacles pour accéder aux services de santé et s'attaquer aux inégalités. Il s'agit de collecter et d'analyser des données ventilées permettant de révéler plus d'informations en rapport avec le genre et les groupes à haut risque, notamment les communautés migrantes, les groupes ethniques marginalisés et les personnes handicapées. Outre des données quantitatives, il est nécessaire d'obtenir des données qualitatives pour fournir un contexte critique des déterminants sociaux du paludisme et des dynamiques culturelles.
Inscrire l'équité comme principe directeur dans l'innovation antipaludique et la découverte de nouveaux produits.
Les utilisateurs des produits, qu'il s'agisse de femmes, de populations mal desservies ou de groupes marginalisés, doivent être impliqués dans la conception des nouveaux outils et l'évaluation des technologies afin de s'assurer que tout est accessible et répond aux besoins des personnes exposées au risque le plus élevé.
Comprendre les barrières liées au genre pour associer le paludisme aux services prénatals
Dans les régions d'endémie palustre ou les zones où la transmission est modérée à élevée, l'OMS recommande un ensemble d'interventions en trois parties pour prévenir et contrôler le paludisme et ses effets durant la grossesse, notamment :
- promotion et utilisation des MII ;
- administration du traitement préventif intermittent pendant la grossesse (TPIp) ;
- diagnostic rapide et traitement antipaludique approprié.
Une évaluation de la compréhension des obstacles liés au genre menée au Cameroun et au Kenya par l'US President's Malaria Initiative (PMI), en collaboration avec les Ministères de la Santé et d'autres partenaires nationaux, a révélé les principaux freins à l'accès et à l'adhésion aux services de prévention du paludisme chez les jeunes filles et les femmes enceintes. En voici les principales conclusions :
- Dans ces deux pays, les partenaires masculins et les belles-mères exercent souvent un contrôle sur les choix des jeunes filles et des femmes au sujet des soins prénatals précoces ;
- De nombreuses jeunes filles et femmes ayant accès aux soins ont eu le sentiment de ne pas être prises au sérieux par les prestataires lorsqu'elles exprimaient leurs inquiétudes, ce qui a eu des répercussions sur leur expérience et leur confiance dans ces services.
Sur la base de ces conclusions, les principales recommandations concernent l'amélioration des compétences des prestataires de santé en matière de communication interpersonnelle respectueuse et la mise en place d'interventions au niveau communautaire pour faire évoluer les normes sociales préjudiciables, qui limitent l'autonomie des femmes dans la prise de décisions concernant leur santé.
Les informations présentées ci-dessus sont extraites de ce document que nous vous invitons à consulter dans son intégralité : Dossier d'information - Principaux messages - Rapport 2024 sur le paludisme dans le monde - 11 décembre 2024 - OMS
6. Données & tendances régionales - Région Afrique
La région Afrique de l'OMS continue de payer le plus lourd tribut au paludisme, cumulant à elle seule 94 % du nombre total des cas de paludisme et 95 % des décès associés au niveau mondial en 2023.
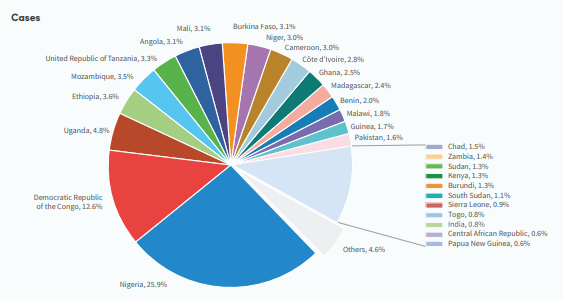
Estimation du nombre de cas de paludisme : en 2023, près de 246 millions de cas de paludisme ont été enregistrés, contre 204 millions en 2000. Cinq pays de la région Afrique ont comptabilisé un peu plus de la moitié des cas à l'échelle mondiale en 2023 : le Nigéria (25,9 %), la République démocratique du Congo (12,6 %), l'Ouganda (4,8 %) l'Éthiopie (3,6 %) et le Mozambique (3,5 %) (Fig. 2.3).
Estimation du nombre de décès dus au paludisme : en 2023, près de 569 000 décès dus au paludisme ont été enregistrés, contre 805 000 en 2000. Suite au pic du nombre de décès associés au paludisme durant la pandémie de COVID-19 (598 000 décès), ce nombre a progressivement diminué chaque année. En 2023, près de 76 % de tous les décès dus au paludisme dans la région ont concerné des enfants de moins de 5 ans, contre 91 % en 2000.
Quatre pays de la région Afrique ont comptabilisé un peu plus de la moitié des décès dus au paludisme dans le monde en 2023 : le Nigéria (30,9 %), la République démocratique du Congo (11,3 %), le Niger (5,9 %) et la République-Unie de Tanzanie (4,3 %). Le Nigéria a cumulé 39,3 % des décès dus au paludisme dans le monde chez les enfants de moins de 5 ans (Fig. 2.3).
 L'incidence de la maladie (cas pour 1 000 habitants exposés au risque de paludisme) a chuté, passant de 356 en 2000 à 227 en 2023. Bien que les taux d'incidence de la maladie aient très peu évolué entre 2019 et 2023, le nombre total de cas a augmenté, conséquence d'une croissance démographique rapide parmi les populations exposées au risque de paludisme (Fig. 2.4 a).
L'incidence de la maladie (cas pour 1 000 habitants exposés au risque de paludisme) a chuté, passant de 356 en 2000 à 227 en 2023. Bien que les taux d'incidence de la maladie aient très peu évolué entre 2019 et 2023, le nombre total de cas a augmenté, conséquence d'une croissance démographique rapide parmi les populations exposées au risque de paludisme (Fig. 2.4 a).
Sur la même période, le taux de mortalité (décès pour 100 000 habitants exposés au risque de paludisme) dans la région a chuté de 63 %, passant de 140 en 2000 à 52 décès en 2023 (Fig. 2.4 b). 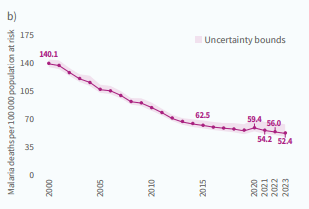
Cas de paludisme et décès évités : plus de 1,7 milliard de cas et 12 millions de décès évités dans le monde depuis 2000 l'ont été dans la région Afrique. Ceci représente 80 % des cas et 94 % des décès évités dans le monde.
Les progrès accomplis dans la région sont très variables
Ces cinq dernières années (2019–2023), huit pays ont enregistré de très fortes hausses de leur nombre de cas de paludisme : l'Éthiopie (+6,9 millions), le Nigéria (+6,8 millions), Madagascar (+4,2 millions), la République-Unie de Tanzanie (+1,9 million), la République démocratique du Congo (+1,8 million), l'Ouganda (+1,3 million), le Mali (+1,4 million) et le Cameroun (+1,2 million) (Fig. 2.4 c).
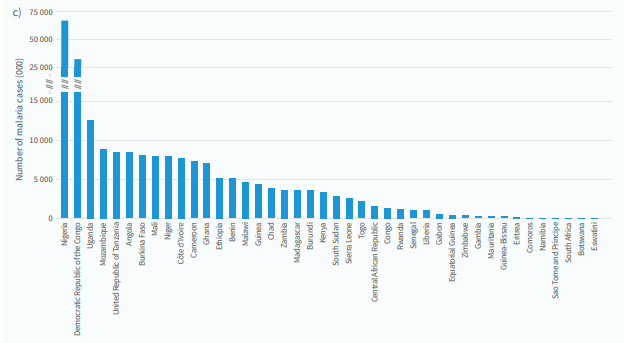
Toutefois, d'autres pays, comme le Rwanda et le Libéria, ont considérablement réduit leur nombre de cas. Au Rwanda, le nombre de cas estimés a chuté de 4,9 millions en 2019 à 749 000 en 2023, soit une baisse de 85 %. Le Libéria a enregistré un recul de 44% sur la période 2017–2023, passant de 1,8 million de cas estimés à 1 million.
Cinq pays de la région Afrique ont signalé moins de 10 décès dus au paludisme en 2023 : le Botswana, les Comores, l'Érythrée, l'Eswatini et Sao Tomé-et-Principe. Depuis 2015, deux pays de la région ont été certifiés exempts de paludisme par l'OMS : l'Algérie (2019) et le Cabo Verde (2023).
L'atteinte des objectifs du GTS dans la région Afrique doit progresser plus rapidement
Même s'ils accusent du retard par rapport aux objectifs fixés pour 2025 dans la Stratégie technique mondiale de lutte contre le paludisme 2016–2030 (GTS) de l'OMS, 21 pays ont réussi à réduire l'incidence de la maladie en 2023 (par rapport à 2015.1 Durant la même période, 34 pays ont enregistré des taux de mortalité en baisse, bien qu'ils n'aient pas encore atteint les niveaux correspondant à l'objectif pour 2025 du GTS en matière de mortalité.2
De 2015 à 2023, la région Afrique dans son ensemble a réduit les taux d'incidence de la maladie et de mortalité de 5 % et 16 %, respectivement. Toutefois, les chiffres de 2023 pour ces deux indicateurs correspondent encore à plus du double des cibles fixées dans la Stratégie mondiale (Fig. 3.4 a & b).
Sur tous les pays d'endémie palustre de la région, seul le Rwanda est en bonne voie d'atteindre l'objectif du GTS de réduire l'incidence de la maladie d'au moins 75 % d'ici 2025 (par rapport aux données de référence de 2015). Sao Toméet-Principe est le seul pays d'endémie en mesure d'atteindre l'objectif de réduction de la mortalité d'ici 2025 fixé dans le GTS, avec zéro décès dû au paludisme en 2023 selon les estimations.
Références :
- Bénin, Burkina Faso, Cameroun, Éthiopie, Gambie, Ghana, Guinée, Guinée équatoriale, Kenya, Libéria, Mali, Mauritanie, Mozambique, Niger, République centrafricaine, République Unie de Tanzanie, Sierra Leone, Soudan du Sud, Togo, Zambie et Zimbabwe.
- Afrique du Sud, Bénin, Botswana, Burkina Faso, Burundi, Cameroun, Congo, Côte d'Ivoire, Éthiopie, Gabon, Gambie, Ghana, Guinée, Guinée-Bissau, Guinée équatoriale, Kenya, Libéria, Malawi, Mali, Mauritanie, Mozambique, Namibie, Niger, Nigéria, Ouganda, Rwanda, Sierra Leone, Soudan du Sud, Tchad, Togo, République démocratique du Congo, République Unie de Tanzanie, Zambie et Zimbabwe.
Les informations présentées ci-dessus sont extraites de ce document que nous vous invitons à consulter dans son intégralité : Dossier d'information - Données & tendances régionales - Rapport 2024 sur le paludisme dans le monde - 11 décembre 2024 - OMS
Pour aller plus loin, nous vous proposons de consulter ces documents :
Combiart® 80/480 mg
1. Dénomination du médicament
Combiart® 80/480 mg, sachets.
2. Composition qualitative et quantitative
Chaque sachet contient :
- Artéméther : 80 mg ;
- Luméfantrine : 480 mg.
3 - Forme pharmaceutique
Granules effervescents.
4. Données cliniques
4.1 Indications thérapeutiques
Combiart® est indiqué pour le traitement du paludisme à Plasmodium falciparum aigu non compliqué chez les adultes.
4.2. Posologie et mode d'administration
Adultes et enfants pesant 35 kg et plus
Pour les patients de 12 ans et plus et de 35 kg de poids corporel et au-dessus, un cours de traitement comprend six doses d'un sachet chacun, c'est-à-dire un total de 6 sachets, donné sur une période de 60 heures comme suit : la première dose d'un sachet, donné au moment du diagnostic initial, devrait être suivie de cinq autres doses d'un sachet chacun donnés à 8, 24, 36, 48 et 60 heures par la suite.
4.3. Contre-indications
Ce médicament ne doit pas être utilisé dans les cas suivants :
- Les malades présentant une hypersensibilité connue aux substances actives ou aux excipients ;
- Les malades souffrant de paludisme grave conformément à la définition de l'OMS ;
- Pendant le premier trimestre de la grossesse (voir mises en garde spéciale et precaution d'emploi) ;
- Les malades qui prennent des médicaments métabolisés par l'enzyme de cytochrome CYP2D6 (ex. flécaïnide, métoprolol, imipramine, amitryptyline, clomipramine) ;
- Les malades présentant des antécédents familiaux de mort subite ou de prolongation congénitale de l'intervalle QTc sur les électrocardiogrammes, ou toute autre condition clinique de prolongation de l'intervalle Qtc ;
- En cas d'antécédent d'arythmie cardiaque symptomatique ou de bradycardie cliniquement appropriée ou avec insuffisance cardiaque congestive accompagnée d' une fraction réduite d'éjection du ventricule gauche ;
- En cas de perturbations d'équilibre de l'électrolyte, par exemple l'hypokaliémie ou l'hypomagnésémie ;
- Les malades qui prennent des médicaments prolongeant l'intervalle QTc. Ces médicaments sont :
- Antiarrhythmiques des classes IA et III ;
- Neuroleptiques, antidépresseurs ;
- Certains antibiotiques incluant certains agents des classes suivantes: fluoroquinolones, macrolides, imidazole et les agents antimycotiques de triazole ;
- Certains antihistaminiques non-sédatifs (terfénadine, astémizole) ;
- Cisapride.
4.4. Mises en garde et précautions d'emploi
L'artéméther et la luméfantrine ne doivent pas être utilisés pendant le premier trimestre de la grossesse dans des situations où d'autres antipaludéens appropriés et efficaces sont disponibles. L'artéméther et la luméfantrine n'ont pas été évalués pour le traitement de paludisme sévère, y compris les cas de paludisme cérébral ou autres manifestations sévères comme l'œdème pulmonaire ou l'insuffisance rénale.
L'artéméther et la luméfantrine n'ont pas été étudiés chez les patients atteints d’insuffisance rénale ou d’ hépatique sévère et par conséquent aucune recommandation ne peut être faite pour ces groupes de patients.
L'artéméther et la luméfantrine ne sont pas indiqués pour le traitement du paludisme dû aux P. vivax, P. malariae ou P. ovale. Il n’ont pas été évalués pour ce traitement, même si certains malades dans les essais cliniques ont une co-infection avec le P. falciparum et P. vivax à la ligne de base.
L'artéméther et la luméfantrine sont actifs face aux étapes sanguines du Plasmodium vivax, mais ne sont pas actifs contre les hypnozoïtes. Par conséquent, un traitement séquentiel avec la primaquine peut être utilisé pour parvenir à l'éradication de l'hypnozoïte.
En raison de données limitées sur la sécurité et l'efficacité, l'artéméther et la luméfantrine ne devraient pas être administrés avec tout autre agent antipaludéen sauf s'il n'y a aucune autre option de traitement. Si l'état d'un malade se détériore pendant qu'il prend l'artéméther et la luméfantrine, le traitement alternatif pour le paludisme devrait commencer immédiatement. Dans ce cas, il est recommandé de contrôler l'électrocardiogramme (ECG) et des mesures devraient être prises pour corriger toutes les perturbations d'électrolyte.
La longue demi-vie d'élimination de luméfantrine doit être prise en compte en administrant la quinine chez les patients précédemment traité avec l'artéméther et la luméfantrine. Si la quinine est administrée après l'artéméther et la luméfantrine, un contrôle sérieux de l'ECG est conseillé. lorsque l'artéméther et la luméfantrine sont administrés après la méfloquine, il est conseillé de surveiller de près la consommation des aliments chez les malades qui ont été antérieurement traités avec l'halofantrine. L'artéméther et la luméfantrine ne devraient être administrés qu'un mois au moins après la dernière dose d'halofantrine. L'artéméther et la luméfantrine ne sont pas indiqués et n'ont pas été évalués pour la prophylaxie.
L'halofantrine, la quinine et la quinidine sont reconnues comme étant la cause de la prolongation de l'intervalle QT. La prolongation asymptomatique d'intervalles QTC par > 30 ms, avec QTC > 450 ms réel chez les hommes et > 470 ms chez les femmes, a été observée à 5% approximativement chez les patients traités avec des doses différentes d'artéméther et de luméfantrine dans des essais cliniques. Il est possible que ces changements soient liés à la maladie. Dans des essais cliniques chez les jeunes, la prolongation asymptomatique d'intervalles QTC > 30 msec a été observée chez 35% des enfants pesant 5-10 kg, 34.1% des enfants pesant 10-15 kg et 23% des enfants pesant 15-25 kg.
La prudence est recommandée lorsque l'artéméther et la luméfantrine sont combinés avec des médicaments exhibant des modèles variables d'inhibition, d’induction ou de compétition pour le CYP3A4.
Les malades qui refusent de s’alimenter pendant le traitement devraient être surveillés de près, le risque de recrudescence pouvant être plus grand.
4.6. Grossesse et allaitement
Grossesse
Catégorie C.
L'efficacité des comprimés d'artéméther / luméfantrine dans le traitement du paludisme aigu non compliqué chez les femmes enceintes n'a pas été établie. Doit être utilisé pendant la grossesse que si l'avantage potentiel justifie le risque potentiel pour le fœtus.
Allaitement
L'avantage de l'allaitement pour la mère et l'enfant doit être pesé contre le risque potentiel pour le nourrisson exposé à l'artéméther et à la luméfantrine par le lait maternel.
4.7 Effets indésirables
La fréquence d'événements indésirables rapportés pendant l'essai clinique avec l'artéméther et la luméfantrine était similaire ou plus basse que celle d'autres médicaments antipaludiques.
L'artéméther et la luméfantrine étaient généralement bien tolérés par les enfants et les adultes, et la plupart des effets indésirables étaient de gravité et de durée bénignes ou modérées. Beaucoup d'effets rapportés vont probablement être rapprochés au paludisme sous-jacent et/ou à une réponse insatisfaisante au traitement plutôt qu'à l'artéméther et la luméfantrine. Pour d'autres rapports, d'autres facteurs alternatifs ont été identifiés comme la cause la plus probable des événements (par exemple, les médicaments concomitants, l'infection concomitante) ou les informations fournies étaient trop rares pour tirer une conclusion.
La relation informelle avec l'utilisation d'artéméther et de luméfantrine ne pouvait pas être exclue pour les effets indésirables suivants :
Les effets indésirables sont classés sous les titres de fréquence, de plus fréquent en premier, utilisant la convention suivante: Très commun (1/10); commun (1/100, < 1/10); non commun 1/1,000, < 1/100); rare (1/10,000, < 1/1,000); très rare (< 1/10,000), y compris les rapports isolés.
Troubles du système immunitaire
Très rarement : Hypersensitivité.
Troubles du système nerveux
- Très commun : Mal de tête, vertige ;
- Commun : Trouble du sommeil, paresthésie ;
- Non commun : Somnolence, contractions involontaires de muscle, hypoesthésie, démarche anormale, ataxie.
Troubles cardiaques
Commun : Palpitation.
Troubles respiratoires, thoraciques et médiastinaux
Commun : Toux.
Troubles gastro-intestinaux
- Très commun : Douleur abdominale, anorexie ;
- Commun : Diarrhée, vomissements, nausée.
Troubles tissulaires cutanés et sous-cutanés
Commun : Prurits, éruption cutanée.
Troubles du tissu musculosquelettique et du tissu conjonctif
Commun : Arthralgie, myalgia.
Troubles généraux et conditions de site d'administration
Commun : Asthénie, fatigue.
La prolongation de QTc asymptomatique a été rapportée chez les adultes, les enfants et les nouveau-nés mais aucune relation causale avec l'artéméther et la luméfantrine ne pouvait être confirmée.
Déclaration des effets indésirables suspectés
Vous pouvez signaler les effets secondaires en visitant le site https://www.strides.com/contact_DS.aspx ou en nous envoyant un courrier électronique à l'adresse drugsafety@strides.com. En signalant les effets secondaires, vous contribuez à fournir davantage d'informations sur la sécurité du médicament.
5. Propriétés pharmacologiques
5.1 Propriétés pharmacodynamiques
Effets pharmacodynamiques
Cette combinaison fixe contient de l' Artéméther et de la Luméfantrine en proportion respective de 1 pour 6. Le site d'action antiparasite des deux composantes est la vacuole digestive du parasite où ils semblent altérer la conversion de l'hème, un intermédiaire toxique produit pendant la dissociation de l'hémoglobine, en hémozoïne non toxique, le pigment du plasmodium. La Luméfantrine est connue pour son interférence avec le processus de polymérisation, pendant que l'artéméther produit des métabolites réactifs suite à l'interaction entre son pont de péroxyde et l'hème ferrique. L'Artéméther et la Luméfantrine bloquent ensuite la synthèse de l'acide nucléique et de protéines intraparasitaires. L'activité antipaludique de la combinaison Artéméther et Luméfantrine est supérieure à celle de l'une ou l'autre des deux substances administrée seule.
5.2 Propriétés pharmacocinétiques
La caractérisation pharmacocinétique de l'artéméther et de la luméfantrine est limitée par le manque d'une formulation intraveineuse et par la variabilité très élevée inter et intra sujet de l'artéméther et des concentrations de plasma de la luméfantrine et des paramètres pharmacocinétiques dérivés (AUC, Cmax).
Absorption
L'artéméther est absorbé assez rapidement avec des concentrations de plasma maximales obtenues environ 2 heures après le dosage. L'absorption de la luméfantrine, un composé hautement lipophilique, commence après un temps de retard de près de 2 heures, avec une concentration de plasma maximale d'environ 6-8 heures après le dosage. L'alimentation augmente l'absorption aussi bien de l'artéméther que de la luméfantrine: chez les volontaires sains, la biodisponibilité relative de l'artéméther a été plus que doublée et celle de la luméfantrine a augmenté plus de seize fois lorsque l'artéméther et la luméfantrine ont été pris après un repas riche en matières grasses comparé au même produit pris dans des conditions de jeûne.
Effet des aliments
L'alimentation augmente l'absorption de la luméfantrine chez les malades atteints de paludisme, bien qu'à un degré moindre (approximativement le double), dû le plus probablement à la teneur en matières grasses inférieure des aliments ingérés par les personnes gravement malades. Les données d'interaction alimentaires indiquent que l'absorption de la luméfantrine dans des conditions de jeûne est très faible (en supposant 100% d'absorption après un repas riche en matières grasses que la même quantité absorbée dans des conditions de jeûne serait < 10% de la dose). Les malades devraient donc être encouragés à prendre les médicaments avec un régime normal aussitôt que les aliments peuvent être tolérés.
Distribution
L'Artéméther et la luméfantrine sont tous les deux fortement liés aux protéines du sérum humain dans les essais in vitro (95.4% et 99.7%, respectivement). Le dihydroartémisinine est aussi lié aux protéines du sérum humain (47-76%). La protéine liée au plasma humain est linéaire
Métabolisme
L'Artéméther est rapidement et largement métabolisé (métabolisme substantiel de premier passage hépatique) dans les essais in vitro et chez l'homme. Les microsomes du foie métabolisent l'artéméther au métabolite principal biologiquement actif, le dihydroartémisinine (deméthylation), principalement à travers l'isoenzyme CYP3A4/5. Ce métabolite a aussi été détecté chez l'homme dans les essais in vivo. Le ratio de l'ASC de l'artéméther/ dihydroartémisinine est 1,2 après une dose unique et 0,3 après 6 doses administrées pendant 3 jours. Les données in vivo indiquent que les artémisinines ont une certaine capacité pour inciter les isoenzymes du cytochrome CYP2C19 et CYP3A4. Le dihydroartémisinine est de nouveau converti en métabolites inactifs. La luméfantrine est N- débutylée, principalement par CYP3A4, dans les microsomes du foie humain. Dans les essais in vivo chez les animaux (chiens et rats), la glucuronidation de la luméfantrine a lieu directement et après biotransformation oxydative. Chez l'homme, l'exposition systémique au métabolite desbutyl- luméfantrine, pour lequel l'effet antiparasitaire in vitro est 5 à 8 fois plus élevé que la luméfantrine, était moins de 1% de l'exposition à la drogue mère. Les données sur la débutyle-luméfantrine ne sont pas disponibles dans le cas spécifique d' une population africaine. Dans les essais in vitro, la luméfantrine inhibe significativement l'activité du CYP2D6 aux concentrations thérapeutiques du plasma.
Élimination
L'artéméther et le dihydroartémisinine sont rapidement éliminés du plasma avec une demi-vie d'élimination d'environ 2 heures. La Luméfantrine est éliminée très lentement avec une demi-vie terminale de 2 à 3 jours chez les volontaires sains et de 4-6 jours chez les malades atteints de paludisme falciparum. Les caractéristiques démographiques comme le sexe et le poids semblent n'avoir pas d' effets cliniquement appropriés sur la pharmacocinétique de l'artéméther et de la luméfantrine. Aucune donnée sur l'excrétion urinaire n'est disponible pour l'homme. Chez les rats et les chiens l'artéméther inchangé n'a pas été détecté dans les excréments et dans l'urine en raison de son métabolisme rapide et de premier passage élevé, mais plusieurs métabolites (non identifiés) ont été détectés tant dans les excréments que dans l'urine. La luméfantrine est éliminée via la bile chez les rats et les chiens, avec une excrétion principalement dans les excréments. Après le dosage oral chez les rats et les chiens, la récupération qualitative et quantitative de métabolites dans la bile et dans les excréments était relativement faible, la plus grande partie de la dose étant récupérée en tant que produit actif.
Pharmacocinétique pour les populations spéciales
Aucun essai pharmacocinétique spécifique n'a été effectué chez les malades atteints d'insuffisance hépatique ou rénale ou chez les enfants ou les patients âgés.
5.3 Données de sécurité préclinique
Sans objet.
6. Données pharmaceutiques
6.1 Liste des excipients
Non renseigné.
6.2 Incompatibilités
Sans objet.
6.3 Durée de conservation
24 mois.
6.4 Précautions particulières de conservation
A conserver à une température ne dépassant pas 30 °C.
A conserver dans l'emballage d'origine à l'abri de la lumière et de l'humidité.
Tenir hors de portée des enfants.
6.5 Nature et contenu de l'emballage extérieur
Boîte de 6 sachets.
6.6 Précautions particulières d'élimination
Pas d'exigences particulières.
7. Titulaire de l'Autorisation de Mise sur le Marché
Strides Pharma Science Limited
Strides House, Opp IIM,
Bilekahalli, Bannerghatta Road,
Bangalore-560 076, INDIA.
8. Date de mise à jour du texte
Mars 2019.
Dernière mise à jour de cette page : 01/02/2024.
Conditions de prescription et de délivrance
Liste I

 Identifiez-vous | Inscription
Identifiez-vous | Inscription
 Identifiez-vous | Inscription
Identifiez-vous | Inscription

 L'incidence de la maladie (cas pour 1 000 habitants exposés au risque de paludisme) a chuté, passant de 356 en 2000 à 227 en 2023. Bien que les taux d'incidence de la maladie aient très peu évolué entre 2019 et 2023, le nombre total de cas a augmenté, conséquence d'une croissance démographique rapide parmi les populations exposées au risque de paludisme (Fig. 2.4 a).
L'incidence de la maladie (cas pour 1 000 habitants exposés au risque de paludisme) a chuté, passant de 356 en 2000 à 227 en 2023. Bien que les taux d'incidence de la maladie aient très peu évolué entre 2019 et 2023, le nombre total de cas a augmenté, conséquence d'une croissance démographique rapide parmi les populations exposées au risque de paludisme (Fig. 2.4 a).






![]() Adresse
Adresse![]() Téléphone
Téléphone